Двс синдром
Содержание:
Этиология
Этиологические формы острого и подострого ДВС-синдрома
-
Инфекционно-септические:
- бактериальные;
- вирусные;
- токсически-шоковый (в том числе при абортах).
-
Травматические и при деструкциях тканей:
- ожоговый;
- синдром длительного сдавления;
- массивные травмы;
- при некрозах тканей и органов (острая токсическая дистрофия печени, некротический панкреатит, острый инфаркт миокарда и др.);
- при остром внутрисосудистом гемолизе, в том числе при переливаниях несовместимой крови;
- при травматичных операциях;
- при массивных гемотрансфузиях;
- при гемобластозах, прежде всего при остром промиелоцитарном лейкозе;
- при острой лучевой болезни.
-
Акушерские и гинекологические:
- при эмболии околоплодными водами (особенно инфицированными);
- при ранней отслойке и предлежании плаценты;
- при атонии и массаже матки;
- при внутриутробной гибели плода и его ретенции;
- при преэклампсии и эклампсии.
- Шоковые (при всех терминальных состояниях).
- В процессе интенсивной химиотерапии.
- При трансплантации органов.
Причинами хронического (затяжного) ДВС-синдрома чаще всего являются следующие виды патологии:
- хрониосепсис, включая затяжной септический эндокардит;
- хронические иммунные и иммунокомплексные болезни;
- хронические вирусные заболевания (гепатит, ВИЧ и др.);
- опухолевые процессы (рак, лимфомы, лейкозы и др.).
Фазы ДВС-синдрома:
I фаза — гиперкоагуляция. Потеря факторов свертывающей системы в процессе обильного кровотечения приводит к удлинению времени образования сгустка и его ретракции, удлинению времени капиллярного кровотечения. Лабораторные показатели: уменьшение времени свертывания крови, тромбинового времени, положительный этаноловый тест.
II фаза — гипокоагуляция. При геморрагическом шоке в фазе спазма венул и артериол (клинические проявления: дегидратация, бледные и холодные кожные покровы, признаки острой почечной недостаточности) в капиллярах развивается расслоение плазмы и форменных элементов — «сладж»-феномен. Агрегация форменных элементов, обволакивание их фибрином сопровождаются потреблением факторов свертывания крови и активацией фибринолиза. Лабораторные показатели: умеренная тромбоцитопения (до 120×109/л), тромбиновое время 60 с и больше, резко положительный этаноловый тест.
III фаза — потребления с активацией местного фибринолиза. Афибриногенемия в сочетании с выраженной активацией фибринолиза. При этой фазе рыхлые сгустки крови в месте кровотечения быстро (в течение 15-20 мин) лизируются на 50 %. Лабораторные показатели: увеличение времени свертывания крови, тромбинового времени, уменьшение тромбоцитов до 100×109/л, быстрый лизис сгустка.
IV фаза — генерализованный фибринолиз. Капиллярная кровь не свертывается, отмечаются паренхиматозное кровотечение, петехиальные высыпания на коже и внутренних органах, гематурия, выпот в синовиальные полости и терминальные изменения в органах и системах.
5.Вторичный плазменный (коагуляционный) гоместаз:внутрений и внешней механизм свертывания.Взаимодействия внешнего и внутренного механизма свертывания.
Коагуляционный
гемостаз.
При ранении
сосудов с высоким давлением остановка
кровотечения начинается также с
сосудисто-тромбоцитарных реакций. Но
образующийся при этом белый тромб не в
состоянии остановить кровотечение.
Начиная с 4ой стадии
сосудисто-тромбоцитарного гемостаза,
включаются биохимические
процессы коагуляционного гемостаза,
который заканчиваетсяпревращением
фибриногена в фибрин. Это превращение
происходит поэтапно. Механизм
свертывания разработан Шмидтом и
развита Моравицем.
Стадии
коагуляционного гемостаза.
I Образование
протромбиназы → тканевой
↓
кровяной
Образование
тканевой протромбиназы.
При ранении
сосудов из мембран разрушенных стенок
и тканей выделяются фосфолипиды,
обладающие тромбопластической
активностью.
При
взаимодействии с факторами плазмы
образуется тканевая протромбиназа. Ее
мало. Под ее влиянием образуется
небольшое количество тромбина. Он
разрушает тромбоциты, вызывает их
необратимую агрегацию и выход в кровь
тромбоцитарных факторов свертывания
крови. Также факторы выделяются из
разрушенных при травме эритроцитов.
При последовательной активации плазменных
факторов свертывания образуется кровяная
протромбиназа. тканевая, кровяная
протромбиназа
↓
II протромбин
→ тромбин
↓
III фибриноген
→ фибрин
IV ретракция
сгустка.
Белки фибрина
под влиянием тромбостенина тромбоцитов
сокращаются, и объем уменьшается на 25
– 30%.
Таким образом,
свертывание крови это последовательный
ферментативный процесс. Катализатором
этих реакций являются фосфолипиды
разрушенных клеточных мембран и
обнаженные волокна коллагена.

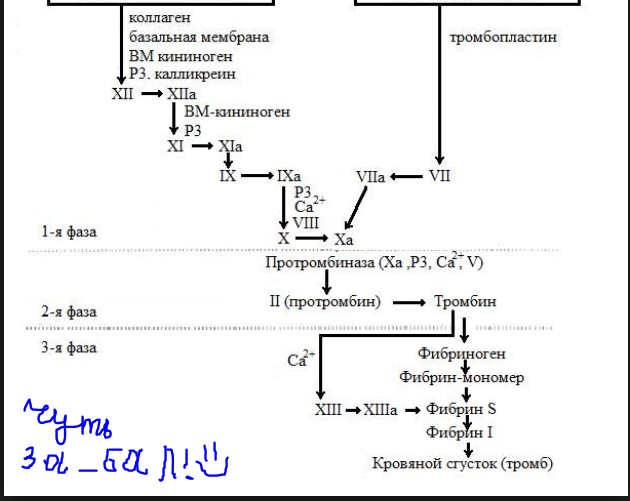

В результате
сложного взаимодействия
перечисленных факторов, а также
ионов Са2+ происходит образование
активного фактора X (фактор Ха).
Затем под
влиянием комплекса факторов: Ха, Va, 3 и
ионов Са2+ (фактор VI) – происходит
образование тромбина из протромбина.
Далее под
влиянием фермента тромбина от фибриногена
отщепляются 2 пептида А и 2 пептида В
(мол. масса пептида А – 2000, а пептида В
– 2400). Установлено, что тромбин разрывает
пептидную связь аргинин–лизин.
После
отщепления пептидов, получивших название
«фибрин-пептиды», фибриноген превращается
в хорошо растворимый в плазме крови
фибрин-мономер, который затем быстро
полимеризуется в нерастворимый
фибрин-полимер. Превращение фибрин-мономера
в фибрин-полимер протекает с участием
фибринстабилизирующего фактора –
фактора XIII в присутствии ионов Са2+.
Известно,
что вслед за образованием нитей фибрина
происходит их сокращение. Имеющиеся в
настоящее время данные свидетельствуют,
что ретракция кровяного сгустка является
процессом, требующим энергии АТФ.
Необходим также фактор 8 тромбоцитов
(тромбостенин). Последний по своим
свойствам напоминает актомиозин мышц
и обладает АТФазной активностью. Таковы
основные стадии свертывания крови.
Классификация ДВС-синдрома
С клинической точки зрения целесообразно выделять 4 стадии ДВС-синдрома:
- Стадии ДВС-синдрома:
- I — стадия гиперкоагуляции
- II — стадия коагулопатии потребления
- III — стадия гипокоагуляции (афибриногенемии или патологического фибринолиза)
- IV — восстановительная стадия
По характеру течения ДВС-синдрома выделяют:
1. Острое (минуты, сутки). Наблюдается при деструктивных процессах в легких, дистрофии печени вирусного или токсического происхождения, некротических или геморрагических панкреатитах, остром внутрисосудистом гемолизе, травматичных операциях, укусах змей и т.д. Эти формы патологии часто сочетаются с септицемией и различными формами суперинфекции.
2. Подострое (1-3 недели). Нередко наблюдается при затяжном септическом процессе, острых лейкозах, повторных массивных трансфузиях крови, воспалительных заболеваниях, отморожениях и других.
3. Хроническое (более 1 месяца). Встречается в основном при онкологических, иммунокомплексных и миелопролиферативных заболеваниях, сердечной недостаточности, деструктивно-склеротических процессах в органах, хроническом гемодиализе, протезировании сосудов и клапанов сердца и др.
4. Рецидивирующее. Наблюдается при деструктивных процессах в органах, особенно связанных с вирулентной микрофлорой (стафилококки, протей, синегнойная палочка) или с токсическим влиянием. При этих формах временные ремиссии сменяются повторными острыми нарушениями гемостаза, приводящими больных к гибели.
По степени нарушения периферического кровотока при ДВС-синдроме выделяют:
1. Компенсированную стадию, которая характеризуется гиперемией кожи, артериальной гипертензией за счет повышения систолического артериального давления, тахикардией. Соотношение между ректальной и кожной температурой не нарушено. Определяется компенсированный метаболический ацидоз и уве-личение гемагокрита на 0,5-7%. Компенсированная стадия определяется в первой фазе ДВС-синдрома
2. Субкомленсированную стадию, характеризующуюся при-знаками централизации кровообращения. Кожа бледная, петехи- альная геморрагическая сыпь, артериальная гипертензия с высоким диастолическим давлением. Нарастает тахикардия. Отмечается несоответствие между кожной и ректальной температурой. Появляются неврологические расстройства, декомпенсирован- ный метаболический ацидоз, увеличение гематокрита на 10%. Эта стадия наблюдается в переходный период и начальный этап фазы гипокоагуляции
3. Декомпенсированную стадию, проявляющуюся развитием пареза периферических сосудов. В большинстве случаев артериальное давление снижено, хотя возможна и значительная артериальная гипертензия. Наблюдается тахикардия или брадикардия, гипертермия, анурия, неврологические расстройства. Выражен геморрагический синдром. Лабораторно определяется состояние смешанного ацидоза, в результате анемии гематокрит снижен. Декомпенсированная стадия наблюдается в фазе глубокой гипокоагуляции.
- Формы ДВС-синдрома:
- геморрагическая
- гипотоническая
- с недостаточностью функций внутренних органов
- макро/микротромботическая
- смешанная
Причины
Патогенез ДВС-синдрома в главной роли имеет появляющиеся факторы в крови, которые активируют кровяную свертываемость или меняют ее агрегационное состояние на клеточном уровне. При процессе размножения тканей, хирургических вмешательствах, которые связаны с техникой разминания органов, применяющейся при «вылущивании» аденомы в тканях предстательной железы, а также в послеродовом периоде при маточном массаже в крови возникают вещества, близкие по свойствам к тканевому тромбопластину. Похожее действие имеется и у бактериальных ферментов, активирующих процесс кровяного свертывания и меняющих агрегационное состояние тромбоцитов. Схожее влияние на организм имеют все инфекции, а также васкулит и возникающие стрессовые ситуации. Кроме этого, в кровяное русло выбрасываются катехоламины и кинины, которые обладают такими же функциями.
Известны три фактора, при которых активируется внутрисосудистая кровяная свертываемость:
- внешний фактор, связанный с действием выброшенных соединений в кровяное русло: тканевый тромблопластин и тромбопластинподобные вещества;
- внутренний фактор, появляющийся после контакта с поврежденными стенками сосудов. Также ДВС-синдром при беременности может активироваться иммунными комплексами;
- клеточная агрегация, появляющаяся вследствие контакта тромбоцитов с поврежденными стенками сосудов, чужеродным телом, а также из-за выброса катехоламинов или возникновения тромбина.
Существует еще один существенный фактор, который приводит к ДВС-синдрому – это сниженные показатели наличия антитромбина III в крови. Данное вещество является основным естественным антикоагулянтом. Здоровые люди имеют колебание уровня данного вещества от 70% до 100%, но при протекании беременности, наличии инфекционного процесса или после хирургического вмешательства уровень антитромбина III может снижаться на 25%, поэтому и возникает риск внутрисосудистого свертывания крови.
Лабораторная диагностика ДВС-синдрома
Цели лабораторной диагностики ДВС-синдрома:
1. Дифферендировка ДВС-синдрома от других патогенетических форм геморрагий
2. Распознавание ДВС-синдрома на ранних доклинических и малосимптомных этапах его развития
3. Распознавание ДВС-синдрома в тех ситуациях, когда он развивается вторично, наслаиваясь на другие нарушения гемостаза
4. Определение в каждом конкретном случае преобладающих механизмов развития ДВС, прослеживание их динамики в процессе болезни и лечения
5. Оценка степени дисфункции отдельных звеньев системы гемостаза и эффективности их устранения
6. Выявление скрытых, малосимптомных хронических форм ДВС-синдрома и своевременная коррекция системы гемостаза и микроциркуляции.
К методам, применяемым для диагностики ДВС-синдрома, предъявляют следующие требования: информативность, сравнительную простоту, оперативность и доступность для клинической практики.
- Исследуемые параметры гемостаза при ДВС-синдроме:
- количества тромбоцитов
- количества тромбоцитов
- протромбинового времени и ПТИ
- эхитоксового времени (тест с ядом эфы)
- тромбинового времени
- активности АТ-III
- концентрации фибриногена
- ПДФ (паракоагуляционные тесты)
- ФАК
| Исследуемый показатель | Норма | I стадия | II стадия | III стадия |
|---|---|---|---|---|
| Количество тромбоцитов, х10^9/л | 150-400 | более 300 | более 150 | менее 100 |
| Время свертывания крови, мин | 8-10 | менее 8 | 10 | более 10 |
| АПТВ, сек | 35-45 | менее 35 | 40 | более 50 |
| АКТ на 10-й минуте, сек | 7-10 | менее 7 | 10-12 | более 12 |
| Протромбиновый индекс, % | 90-105 | более 105 | 90-100 | менее 90 |
| Фибриноген, г/л | 2-4 | более 3-4 | 2-3 | менее 2 |
| Тромбиновое время, сек | 12-17 | менее 12 | 15-20 | более 20 |
| AT-III, % | 80-120 | 80-90 | 75-80 | 30-60 |
| Этаноловый тест | отрицательный | положительный | положительный | положительный/отрицательный |
| Протамин-сульфатный тест | отрицательный | положительный | положительный | положительный |
| ФАК, мин | 150-200 | менее 150 | менее 100 | более 200 |
| Фактор XIII, % | 80-120 | 130 | 110 | менее 50 |
| ПДФ, мг/л | менее 2 | более 20 | более 15 | более 10 |
| Наличие обломков эритроцитов в мазке крови («легкие» эритроциты) | нет | единицы в препарате | единицы в препарате | единицы в поле зрения |
Необходимо подчеркнуть, что динамика (и даже спектр) коагулогических. показателей ДВС-синдрома зависит от характера его клинического течения (острое, подострое, хроническое) и конкретного патологического процесса, вызвавшего развитие ДВС. Так, например, острый ДВС-синдром характеризуется ранним снижением активности фактора ХIII плазмы, увеличением в крови ПДФ и продуктов паракоагуляции. Подострое течение ДВС-синдрома далеко не всегда сопровождается тромбоцитопенией. Хроническое течение ДВС также может характеризоваться отсутствием тромбоцитопении, более того, в ряде случаев имеют место тромбоцитозы.
Лабораторно-диагностический контроль эффективности терапии ДВС-синдрома осуществляется на основании динамики гемостазиологических параметров. При остром ДВС-синдроме тесты целесообразно повторять в первые сутки лечения каждые 2-3 часа. Тенденция к их нормализации позволяет судить об эффективном лечении ДВС. При этом наибольшую диагностическую информативность имеет динамика следующих показателей: времени свертывания крови, уровня АТ-III, ПДФ, фибриногена, ФАК.
При диагностике хронического ДВС-синдрома раннее выявление ДВС по результатам наиболее распространенных исследований весьма маловероятно. В этом случае, а также для контроля эффективности лечения целесообразно динамически определять АПТВ, АКТ, уровень фибриногена, ПДФ, АТ-III, ФАК и обязательно дополнять этот перечень определением в динамике числа и функции тромбоцитов, а также тромбоцитарного фактора 4.
Это может быть полезным для Вас:
Лечение ДВС-синдрома
Терапию ДВС-синдрома осуществляет врач, столкнувшийся с данной патологией (то есть лечащий врач) вкупе с реаниматологом. При хроническом течении ДВС-синдрома его лечением занимается терапевт с гематологом.
В первую очередь необходимо устранить причину ДВС-синдрома. Например, при сепсисе назначается антибактериальная и трансуфизионная (внутривенное вливание препаратов крови) терапия, при травматическом шоке – адекватное обезболивание, иммобилизация, оксигенация и раннее хирургическое вмешательство. Или при опухолевых заболеваниях – химио- и радиотерапия, при инфаркте миокарда – купирование болевого синдрома, восстановление сердечного ритма и гемодинамики, при акушерской и гинекологической патологии радикальные меры (экстирпация матки, кесарево сечение).
Восстановление гемодинамики и реологических свойств крови осуществляется путем инфузионно-трансфузионных вливаний.
Показано вливание свежезамороженной плазмы, которая не только восстанавливает объем циркулирующей крови, но и содержит все факторы свертывания.
Также вводят кристаллоидные (физ. раствор, глюкоза) и коллоидные растворы (полиглюкин, реополиглюкин) в отношении 4/1 и белковые препараты крови (альбумин, протеин).
Назначается антикоагулянт прямого действия – гепарин. Доза гепарина зависит от стадии ДВС-синдрома (в 1 – 2 фазы она значительная). При значительной анемии переливается свежая (не более 3 суток) эритроцитарная масса.
В лечении тяжелого генерализованного ДВС-синдрома применяют фибриноген и концентраты свертывающих факторов крови (криопреципетат). Используют игинбиторы протеолиза – антипротеазы, для подавления тканевых протеаз, которые высвобождаются при повреждении клеток (контрикал, трасилол, гордокс). Также назначаются кортикостероиды (гидрокортизон, дексаметазон), так как они повышают свертываемость крови.
Параллельно ведется борьба с полиорганной недостаточностью (поддержка функций легких, почек, желудочно-кишечного тракта, надпочечников). Во 2 – 4 фазах ДВС-синдрома для восстановления местного гемостаза применяют смесь из аминокапроновой кислоты, сухого тромбина, этамзилата натрия и адроксона. Данную смесь вводят в брюшную полость через дренажи, перорально, в виде тампонов в полость матки и влагалища, а смоченные раствором салфетки наносят на рану.
Весь процесс интенсивной терапии занимает 1 – 5 суток (в зависимости от тяжести ДВС-синдрома), а последующее лечение продолжается до полного или практически полного восстановления всех полиорганных нарушений.
ДВС-синдром у детей
Группу риска по возникновению признаков ДВС-синдрома составляют дети в периоде новорожденности и на долю этой патологии приходится не менее 15%. В отличие от взрослых, дети страдают ДВС-синдромом, обусловленным тяжелой формой внутриутробной инфекции и вирусным поражением организма. Кроме того, провокаторами возникновения нарушений в системе гемостаза может выступать длительный период гипотермии, тяжелая внутриутробная гипоксия плода, а также выраженное ацидотическое состояние.
При всех этиопатогенетических типах ДВС-синдрома, которые встречаются в детском возрасте, пусковым механизмом возникновения нарушений в системе гемостаза является сердечно-сосудистый шок, в результате чего происходит прогрессирующее повреждение эндотелия сосудистой стенки и выделение в кровь факторов активации агрегации тромбоцитов.
В патогенезе развития ДВС-синдрома у детей принято выделять следующие процессы:
— образование большого количества тромбина или так называемый «протеолитический взрыв»;
— тотальное повреждающее воздействие на сосудистую стенку эндотоксинами;
— период гиперкоагуляции за счет стимуляции как внутреннего, так и внешнего путей процесса коагуляции;
— одновременное образование огромного количества фибриновых тромбов в просвете сосудов мелкого калибра и изменение реологических свойств крови;
— полиорганная недостаточность, спровоцированная тотальной тканевой гипоксией;
— коагулопатия и тромбоцитопения;
— нарушение первичного и вторичного гемостаза, обусловленное патологическим фибринолизом.
Развитие клинических проявлений зависит от того, на какой патофизиологической стадии развития находится процесс нарушения системы гемостаза.
Так, для гиперкоагуляционной фазы не характерно проявление специфических симптомов ДВС-синдрома и в большей степени клиническая симптоматика обусловлена проявлением заболевания, явившегося первопричиной развития данного осложнения. В некоторых случаях может наблюдаться акроцианоз кожных покровов, увеличение частоты сердечных сокращений и частоты дыхательных движений, склонность к гипотонии, затрудненное мочеиспускание. При объективном осмотре пальпаторно определяются увеличенные размеры печени и селезенки.
В коагулопатической фазе, при которой отмечается выраженное снижение содержания тромбоцитов в крови, кожные покровы приобретают синюшный оттенок, и развивается клиника геморрагического шока, обусловленного кровотечением из различных источников. Нередкой ситуацией в этой фазе является возникновение кровоизлияний в головной мозг, сопровождающихся глубокими нарушениями очагового и общемозгового характера. На этой стадии значительно возрастает риск летального исхода, составляющий не менее 50% случаев, однако при своевременно оказанной медицинской помощи можно добиться благоприятного исхода заболевания.
В случае применения адекватного объема лечебных мероприятий наступает восстановительная фаза, для которой характерно купирование признаков кровотечения и частичное или полное восстановление утраченной функции поврежденных органов.
При выборе метода медикаментозной коррекции нарушений системы гемостаза у детей, необходимо отдавать предпочтение этиопатогенетической направленности терапии, то есть лечение в первую очередь должно обеспечивать полное устранение первопричины возникновения ДВС-синдрома и учитывать стадию его развития.
Так в период гиперкоагуляционной фазы целесообразно применение трансффузионной терапии, для чего используется раствор свежезамороженной плазмы методом внутревенно-капельного введения с расчетом 10мл на кг веса в сочетании с 2% раствором Пентоксифиллина в дозе 0,1 мл. Полная микроциркуляторная блокада является обоснованием для назначения ингибиторов моноаминооксидазы (внутривенное введение Допамина в дозе 5 мкг/кг).
В фазе коагулопатии и тромбоцитопении патогенетически обоснованными являются препараты, содержащие фактор свертывания VIII, а также заменное переливание эритроконцентрата и тромбоцитарной массы. На данном этапе продолжается инфузионная терапия с целью восполнения необходимого количества жидкости и подкожное введение Гепарина в дозе 25 ЕД/кг через каждые 8 часов под постоянным контролированием показателей коагулограммы.
Восстановительный период требует применения симптоматических групп препаратов, направленных на восстановление функции того или иного органа. В некоторых случаях в этой фазе применяются препараты тромболитической терапии, направленные на устранение тромбов крупных размеров.
Причины
Тяжелые вирусные заболевания могут стать причиной ДВС-синдрома
Данный синдром почти никогда не бывает самостоятельным заболеванием, он часто возникает как осложнение других заболеваний. И чем серьезнее основное заболевание, тем серьезнее проявляется этот синдром. Более того, даже если сопутствующее заболевание затрагивает всего один орган, другие органы и системы организма будут вовлечены при развитии тромбогеморрагического синдрома. Предрасполагающими факторами развития данного синдрома могут быть:
- Тяжелые вирусные, бактериальные, грибковые инфекционные и воспалительные заболевания;
- Аутоиммунные патологии;
- Онкологические заболевания;
- Послеоперационные осложнения;
- Ответ организма при переливании компонентов несовместимой группы крови;
- Резкое падение артериального давления;
- Септицемия;
- Длительный прием антикоагулянтов или лекарственных средств, увеличивающих риск образования сгустков крови;
- Острое отравление змеиным ядом и некоторыми химическими веществами.

Патология беременности может предрасполагать к синдрому
Основными предпосылками возникновения этого синдрома у беременных являются:
- Отделение плаценты от матки раньше времени;
- Большие потери крови из-за ушибов или травм;
- Повреждения родового канала или разрыв самой матки;
- Нахождение в утробе мертвого плода длительное время;
- Резус-конфликт плода и матери;
- Тяжелое течение беременности, сопровождающееся гестозами, преэклампсией, эклампсией;
- Длительная стимуляция родов.
В группе риска — новорожденные с родовой травмой
Часто тромбогеморрагический синдром наблюдается у новорожденных, при этом основные причины следующие:
- Гипоксия плода, т.е. дефицит кислорода;
- Гипотермия тела женщины;
- Родовая травма;
- Осложненный курс беременности.
У подростков и молодых людей частыми предрасполагающими причинами бывают такие, как:
- Политравмы;
- Сильное постинфекционное обезвоживание;
- Осложнения воспалительных заболеваний, которые нарушают функцию почек и печени.
Любые изменения способности крови к свертыванию возможно обнаружить, сделав коагулограмму.
I. Полнокровие.
Артериальное
— усиливается приток крови к органу
или части органа. Внешне орган красный,
повышение температуры органа (он теплый).
Плетора
— общее артериальное полнокровие.
Причины:
1.
Воспалительные реакции.
2.
Усиленно работающие коллатерали.
Венозный
застой — пассивный процесс. Отек ткани,
плазморрагия, диапедезные кровоизлияния,
дистрофические изменения клеток в
результате гипоксии, язвы.
При
хроническом процесса развиваются
атрофические и склеротические процессы.
Застой
при нарушении оттока.
Местная
— закупорка вены тромбом, воспалительные
заболевания, развитые венозные
коллатерали.
Общая
— острая (острая сердечная недостаточность,
острый инфаркт миокарда, асфиксия);
хроническая (морфологическое выражение
хронической сердечной недостаточности.
Исход ПС, инфаркта, кардиосклероз).
Наблюдаются
изменения в:
— легких
— увеличенные, бурого цвета, плотные
(бурая индурация легких). В результате
расширения капилляров, из них выходят
эритроциты — образуются сидерофаги
(клетки “сердечных пороков”). Они
находятся в альвеолярных перегородках
и внутри альвеол.
— печень.
Полнокровна вначале, затем приобретает
мускатный цвет, на желтом фоне прожилки
красного цвета, атрофия печеночных
клеток, в центре жировая дистрофия. В
синусоидах разрастается соединительная
ткань (капилляризация синусоидов), т.е.
идет разрастание фибробластов.
В
подкожной клетчатке развиваются отеки.
Почки, селезенка, кожа — цианотическая
индурация.
II.
Стаз.
Остановка и застой крови в мелких
сосудах.
Причины:
1.
Физические факторы
2.
Химические факторы
3.
Инфекции
4.
Воспалительные процессы
5.
Сердечная недостаточность
6.
Нейротрофические и дисциркуляторные
нарушения
Стадии:
1.
Замедление тока крови (предстаз)
2.
Стаз
3.
Постстатические изменения (тромбы)
Стаз
необратим. Клинически стаз — кома.
Slage-феномен
— сгущение крови в капиллярах, эритроциты
приближаются друг к другу.
III.
Тромбоз.
Прижизненное свертывание крови в
просвете сосуда или сердца. Сверток
крови при этом носит название тромба.
Тромбоз
может быть благоприятным процессом.
1.
Агглютинация тромбоцитов
2.
Коагуляция фибриногена и образование
фибрина.
3.
Агглютинация эритроцитов
4.
Преципитация белков плазмы (осаждение)
Вначале
происходит агрегация тромбоцитов.
Происходит травма тромбоцитов. Они
меняют свою форму.
агрегация
тромбоцитов
“травма”
тромбоцитов
высвобождение
гиаломера (ЛПК)
агглютинация
тромбоцитов
дегрануляция
серотонин ТФП
активный
тромбопластин (тромбокиназа)
протромбин+Ca2++
тромбокиназа тромбин
фибириноген+тромбин
фибрин-мономер (грануломер ретрактазин
пластинок)
отжатие
фибринового свертка (агглютинация
эритроцитов, лейкоцитов и белков плазмы
крови)
преципитация
белков
Внешний
вид тромба:
макроскопически — суховатый, интимно
спаян со стенкой сосуда. Посмертные
свертки — на спаяны со стенкой сосуда.
Тромбы
бывают:
1.
Красные (в венах) — фибрин + эритроциты
2.
Белые (в артериях) — лейкоциты, фибрин,
тромбоциты
3.
Смешанные (чаще в артериях)
Имеют
головку, тело и хвостик.
В
сосудах МЦР тромбы состоят из фибрина
и форменных элементов. Тромбы в МЦР
появляются при ДВС-синдроме, стрессах.
Маразтические
(?) тромбы — при истощении, дегидратации
в синусах твердой мозговой оболочки, в
конечностях.
Исходы:
1.
Аутолиз асептический (под действием
ферментных систем)
2.
3.
Васкуляризация
4.
Реканализация — образование в тромбе
сосудистой полости.
5.
Петрификация (флебоилит — венный камень)
6.
Септический аутолиз (расплавление
тромба)
Закрытие
просвета тромба — приводит к некрозу.
Причины
тромбообразования:
1.
Состояние сосудистой стенки (атеросклероз,
воспалительные заболевания, аллергические
изменения). Поврежденный эндотелий.
2.
Нарушение кровотока (замедление,
извращение — завихрения в валексах).
3.
Главная причина — изменения качества
крови. Недостаток гепарина, антитромбина,
избыток свертывающих факторов и т.д.
Заболевания
при гипертромбоцитозах:
1.
Некоторые инфекции
2.
Спленэктомия
3.
Операция
4.
Роды
ДВС-синдром
— синдром диссеминированного
внутрисосудистого свертывания
(коагулопатия, тромбогеморрагический
синдром).
Характеризуется
образование тромбов в сосудах МЦР с
кровоизлияниями, с несвертыванием в
крупных сосудах.
Стадии:
1.
Гиперкоагуляция
2.
Переходная (коагулопатия потребления)
3.
Гипокоагуляции
4.
Восстановление или исход и осложнения
ДВС-синдром
развивается при:
1.
Переливании несовместимой крови
2.
Эмболия околоплодными водами
3.
Шоковые реакции
4.
Генерализованные поражения сосудистых
стенок
5.
Инфекционные заболевания
6.
Сепсис