Анализ факторы свертывания крови таблица
Содержание:
- Системы и факторы
- Фактор Хагемана (фактор XII, фактор контакта)
- Первая фаза свертывания крови
- Процесс свёртывания крови
- Первичный гемостаз. Первичные физиологические механизмы свертывания крови
- Фазы свертывания
- Как проходит свертывание
- Эритроциты
- Чем опасно нарушение?
- Гемостаз в организме женщины
- Лечение
- Как происходит свертывание крови?
- Какие показатели определяет анализ
Системы и факторы
Выделяют тринадцать плазменных факторов влияющих на свертывание крови. Каждый из них играет свою роль, и если с одним идет нарушение, страдает вся цепочка. Их наглядно демонстрирует следующая таблица:
| Наименование | Свойства и действия |
|
Фибриноген |
Отвечает за выделение фибрина с целью формирования сетчатой базы тромба. Продуцируется в тканях дыхательной системы, селезенке, костно-мозговых трубках и лимфапродуцирующих узлах человека |
|
Протромбин |
Возникают молекулы за счет К в печени |
|
Тромбопластин |
Играет важную роль в провокации работы протромбина. Концентрируется внутри систем организма |
|
Са (кальций) |
Обязательный фактор для загустевания крови. Важен на всех стадиях |
|
Проакцелерин |
Дает толчок к запуску биоперекрещиванию протромбина и произведению протромбиназы |
|
Акцелерин |
Значимым является только проакцелерин, он продуцируется при наличии тромбина |
|
Проконвертин |
Пик действия отмечается на стартовой позиции цепочки коагуляции при совмещении с пораженной тканью. Участвует в синтезе тромбина и поверхностной протромбиназы |
|
А-глобулин |
Фактор свертывания крови VIII отвечает за реформацию протромбина |
|
В-глобулин |
Важнейшая единица всей цепочки. Нехватка провоцирует кровоизлияния |
|
Стюарта-Прауэра |
Основополагающее звено по продуцированию протромбиназы. Зависит от 3-его, 7-ого и 9-ого факторов |
|
Компонент Розенталя |
Из него идет формирование тромбопластина. Приводится в действие 12-ым фактором |
|
Хагемана |
Необходим для того, чтобы начал действовать 11-ый фактор |
|
Фибриназа |
Подталкивает кровь к биологически правильному свертыванию. Нехватка провоцирует внутричерепные кровоизлияния |
Обратите внимание.
В процессе коагуляции участвуют и другие компоненты плазменного тромбирования: это молекулярные части Фицджеральда, Флетчера и Виллебранда.
В биологическом действии участвует множество систем. Часть их занимает спящую позицию и появляется только при возникновении определенных условий. Чтобы перевести их из неактивной формы в активную, требуется пусковой механизм или стимулятор. Таким стимулятором и является тромбопластин.
Тромбопластин появляется (выходит) в момент повреждения тканей (кожи, сосудов, проч.), и его выход носит защитный характер. Тромбопластин останавливает кровотечение, спасая таким образом человеку жизнь.
Цитокины – это одни из тех клеток, которые получают сигнал от иммунной системы о том, что ей нужна помощь. Цитокины, в свою очередь, передают сигнал тревоги дальше, уже тем клеткам, которые начнут искать, где возникла проблема и что с ней делать. Вместе с другими клетками они образуют микроэндокринную систему. С помощью цитокинов происходит общение между ними и клетками иммунной системы. После выполнения своей задачи цитокины живут какое-то время и отмирают.
Тромбоциты – это кровяные тельца-пластинки, которые являются элементами крови. При повреждении кожных покровов тромбоциты оказывают кровоостанавливающее действие, «закрывая» рану. Каждый тромбоцит содержит в себе адренозиндифосфорат, тромбин, тромоксан и другие, которые называются тромбоцитарными факторами. Они защищают организм от вирусов и бактерий, которые могут попасть в рану извне.
Фактор Хагемана (фактор XII, фактор контакта)
Фактор Хагемана (фактор XII, фактор контакта) синтезируется в печени, вырабатывается в неактивном состоянии, период полураспада – 50 – 70 часов. Содержание фактора в плазме составляет около 0,03 г/л. Кровоточивость не возникает даже при очень глубоком дефиците фактора (менее 1%).
Активируется при соприкосновении с поверхностью кварца, стекла, целлита, асбеста, карбоната бария, а в организме – при контакте с кожей, волокнами коллагена, хондроитинсерной кислотой, мицеллами насыщенных жирных кислот. Активаторами фактора XII являются также фактор Флетчера, калликреин, фактор XIа, плазмин.
Первая фаза свертывания крови
Плазменные факторы свертывания крови – совокупность неактивных ферментов и неферментных соединений, которые обитают в плазменной части крови и кровяных пластинках. Для свертывания крови помимо прочего необходимы ионы Са (IV) и витамин К.
Когда повреждаются ткани, разрываются сосуды, идет гемолиз клеток крови включается череда реакций с активацией ферментов. Начало активации обусловлено взаимодействием плазменных факторов свертывания с разрушенными тканями (внешний тип активации коагуляции), частями эндотелия и форменных элементов (внутренний тип активации коагуляции).
Внешний механизм
Из оболочки разрушенных клеток в кровяное русло попадает специфический белок – тромбопластин (III фактор). Он активирует VII фактор, присоединяя молекулу кальция, эта новообразованная субстанция воздействует на X фактор для последующей активации. После X фактор соединяется с тканевыми фосфолипидами и V фактором. Сформировавшийся комплекс за пару секунд преобразовывает долю протромбина в тромбин.
Внутренний механизм
Под действием разрушенного эндотелия или форменных элементов активируется XII фактор, который после воздействия кининогена плазмы активирует XI фактор. XI действует на IX фактор, который после перехода в активную фазу формирует комплекс: «коагуляционный фактор (IX) + Антигемофильный фактор В (VIII) + тромбоцитарный фосфолипид + ионы Са (IV)». Он активирует фактор Стюарта-Прауэра (X). Активированный X совместно с V и ионами Са действуют на фосфолипидную оболочку клетки и формируют новое образование – кровяную протромбиназу, которое обеспечивает переход протромбина в тромбин.
Внешний механизм свертывания крови длится примерно 15 секунд, на внутренний приходится от 2 до 10 минут. Завершается эта фаза свертывания образованием тромбина из протромбина.
Протромбин синтезируется в печени, чтобы синтез осуществлялся нужен витамин К, который поступает с едой и накапливается в печеночной ткани. Таким образом, при поражении печени или недостатке витамина К, система свертывания крови не функционирует нормально, и часто возникает неконтролируемый выход крови из сосудистого русла.
Процесс свёртывания крови
Классическая схема свёртывания крови по Моравицу (1905 год)
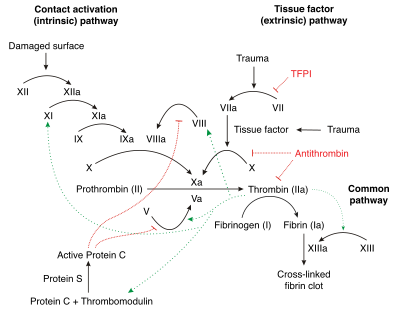
Схема взаимодействия факторов свёртывания крови
Процесс свёртывания крови представляет собой преимущественно проферментно-ферментный каскад, в котором проферменты, переходя в активное состояние, приобретают способность активировать другие факторы свёртывания крови.
В самом простом виде процесс свёртывания крови может быть разделён на три фазы:
- фаза активации включает комплекс последовательных реакций, приводящих к образованию протромбиназы и переходу протромбина в тромбин;
- фаза коагуляции — образование фибрина из фибриногена;
- фаза ретракции — образование плотного фибринового сгустка.
Данная схема была описана ещё в 1905 году Моравицем и до сих пор не утратила своей актуальности.
В области детального понимания процесса свёртывания крови с 1905 года произошёл значительный прогресс. Открыты десятки новых белков и реакций, участвующих в процессе свёртывания крови, который имеет каскадный характер. Сложность этой системы обусловлена необходимостью регуляции данного процесса.
Современное представление с позиций физиологии каскада реакций, сопровождающих свёртывание крови, представлено на рис. 2 и 3.
Вследствие разрушения тканевых клеток и активации тромбоцитов высвобождаются белки фосфолипопротеины, которые вместе с факторами плазмы Xa и Va, а также ионами Ca2+ образуют ферментный комплекс, который активирует протромбин. Если процесс свёртывания начинается под действием фосфолипопротеинов, выделяемых из клеток повреждённых сосудов или соединительной ткани, речь идёт о внешней системе свёртывания крови (внешний путь активации свёртывания, или путь тканевого фактора). Основными компонентами этого пути являются 2 белка: фактор VIIа и тканевый фактор, комплекс этих 2 белков называют также комплексом внешней теназы.
Если же инициация происходит под влиянием факторов свёртывания, присутствующих в плазме, используют термин внутренняя система свёртывания. Комплекс факторов IXа и VIIIa, формирующийся на поверхности активированных тромбоцитов, называют внутренней теназой. Таким образом, фактор X может активироваться как комплексом VIIa—TF (внешняя теназа), так и комплексом IXa—VIIIa (внутренняя теназа). Внешняя и внутренняя системы свёртывания крови дополняют друг друга.
В процессе адгезии форма тромбоцитов меняется — они становятся округлыми клетками с шиповидными отростками. Под влиянием АДФ (частично выделяется из повреждённых клеток) и адреналина способность тромбоцитов к агрегации повышается. При этом из них выделяются серотонин, катехоламины и ряд других веществ. Под их влиянием происходит сужение просвета повреждённых сосудов, возникает функциональная ишемия. В конечном итоге сосуды перекрываются массой тромбоцитов, прилипших к краям коллагеновых волокон по краям раны.
На этой стадии гемостаза под действием тканевого тромбопластина образуется тромбин. Именно он инициирует необратимую агрегацию тромбоцитов. Реагируя со специфическими рецепторами в мембране тромбоцитов, тромбин вызывает фосфорилирование внутриклеточных белков и высвобождение ионов Ca2+.
При наличии в крови ионов кальция под действием тромбина происходит полимеризация растворимого фибриногена (см. фибрин) и образование бесструктурной сети волокон нерастворимого фибрина. Начиная с этого момента в этих нитях начинают фильтроваться форменные элементы крови, создавая дополнительную жёсткость всей системе, и через некоторое время образуя тромбоцитарно-фибриновый сгусток (физиологический тромб), который закупоривает место разрыва, с одной стороны, предотвращая потерю крови, а с другой — блокируя поступление в кровь внешних веществ и микроорганизмов.
На свёртывание крови влияет множество условий. Например, катионы ускоряют процесс, а анионы — замедляют. Кроме того, существуют вещества как полностью блокирующие свёртывание крови (гепарин, гирудин и другие), так и активирующие его (яд гюрзы, феракрил).
Врождённые нарушения системы свёртывания крови называют гемофилией.
Первичный гемостаз. Первичные физиологические механизмы свертывания крови
Первичный гемостаз — это образование слабой тромбоцитарной пробки, которая достигается в четыре фазы: вазоконстрикция, адгезия тромбоцитов, активация тромбоцитов и агрегация тромбоцитов.
Вазоконстрикция — это начальная реакция, когда происходит повреждение сосуда. Вазоспазм кровеносных сосудов возникает в первую очередь в ответ на повреждение сосудистой сети. Этот спазм сосудов, в свою очередь, стимулирует сужение сосудов. Вазоконстрикция главным образом опосредована эндотелином-1, мощным вазоконстриктором, который синтезируется поврежденным эндотелием. Поврежденный эндотелий экспонирует субэндотелиальный коллаген, фактор Виллебранда (vWF), высвобождает АТФ и медиаторы воспаления. vWF синтезируется мегакариоцитами, которые позже накапливаются в а-гранулах тромбоцитов. Тела Вейбеля-Паладе эндотелия также синтезируют vWF. Это сочетание воздействия vWF, субэндотелиального коллагена, АТФ и медиаторов воспаления, которые обеспечивают ворота во вторую фазу первичного гемостаза, адгезию тромбоцитов.
Ключевой момент в физиологии свертывания крови — это адгезия тромбоцитов.
Адгезия тромбоцитов — это процесс, посредством которого тромбоциты прикрепляются к обнаженному субэндотелиальному vWF. После повреждения сосудов тромбоциты начинают перемещаться вдоль стенок сосудов и прилипать к участкам обнаженного субэндотелиального коллагена и vWF. Мембраны тромбоцитов богаты рецепторами G-белка (Gp), расположенными внутри фосфолипидного бислоя. В частности, именно рецептор Gp Ib-IX на тромбоцитах, который связывается с vWF в эндотелии, создает первоначальную связь между ними. После связывания в третьей фазе первичного гемостаза может произойти целый ряд событий, приводящих к активации тромбоцитов.
Важным этапом свертывания крови в организме человека и животных является активация тромбоцитов.
Активация тромбоцитов состоит из того, что тромбоциты претерпевают два специфических события после того, как они прилипли к открытой vWF (т. е. к поврежденному участку сосуда). Во-первых, тромбоциты будут подвергаться необратимому изменению формы от гладких дисков до мульти-псевдоподальных пробок, что значительно увеличивает их площадь поверхности. Во-вторых, тромбоциты секретируют свои цитоплазматические гранулы.
Активация тромбоцитов опосредуется через тромбин двумя механизмами. Тромбин непосредственно активирует тромбоциты через протеолитическое расщепление, связывая активированный протеазой рецептор. Тромбин также стимулирует высвобождение гранул тромбоцитов, которые включают серотонин, активирующий тромбоцитарный фактор и аденозиндифосфат (АДФ). АДФ является важным физиологическим агонистом, который хранится именно в плотных гранулах тромбоцитов. Когда АДФ высвобождается, он связывается с рецепторами P2Y1 и P2Y12 на мембранах тромбоцитов. P2Y1 индуцирует изменение формы псевдоподий и способствует агрегации тромбоцитов. P2Y12 играет важную роль в индуцировании каскада свертывания крови. Когда АДФ связывается со своими рецепторами, он индуцирует экспрессию комплекса Gp IIb/IIIa на поверхности мембраны тромбоцитов. Комплекс Gp IIb/IIIa представляет собой кальцийзависимый коллагеновый рецептор, который необходим для адгезии тромбоцитов к эндотелию и агрегации тромбоцитов. Одновременно тромбоциты синтезируют тромбоксан А2 (TXA2). TXA2 дополнительно усиливает вазоконстрикцию и агрегацию тромбоцитов (следующий этап процесса первичного гемостаза). Процесс активации тромбоцитов подготавливает местную среду для агрегации тромбоцитов.
Ключевым моментом в реализации физиологических механизмов свертывания крови является феномен агрегации тромбоцитов.
Агрегация тромбоцитов начинается сразу после активации тромбоцитов. После активации рецепторы Gp IIb/IIIa присоединяются к vWF и фибриногену. Фибриноген находится в циркуляции и образует связь между рецепторами Gp IIb/IIIa тромбоцитов, чтобы соединить их друг с другом. Это в конечном счете формирует слабую тромбоцитарную пробку.
В конечном счете, первичный гемостаз позволяет кульминации слабой тромбоцитарной пробки временно защитить от кровоизлияния до тех пор, пока во вторичном гемостазе не произойдет дальнейшая стабилизация фибриногена до фибрина через тромбин.
Фазы свертывания
 Визуально процесс свертывания крови можно представить в виде проферментно-ферментного каскада. При этом его элементы находятся в активном состоянии. Для подробного рассмотрения процессы свертывания можно разделить на три этапа. Основные фазы:
Визуально процесс свертывания крови можно представить в виде проферментно-ферментного каскада. При этом его элементы находятся в активном состоянии. Для подробного рассмотрения процессы свертывания можно разделить на три этапа. Основные фазы:
- Активизация. Представлена комплексом реакций, провоцирующих образование протромбиназы. Завершается переходом протромбина в тромбин.
- Коагуляция. Заключается в образовании фибрина из фибриногена.
- Ретракция. Состоит в формировании плотного фибринового сгустка.
Биохимическая цепочка свертывания представляет собой реакцию превращения растворимых белков, полимеризующихся в сетку. Отдельные процессы представлены цепочками каскада, сохраняющими физический смысл. Вспомогательные реакции обеспечивают регуляторную функцию, способствуя превращению фибриногена в фибрин в необходимый момент.
Внимание!
Важным компонентом крови, участвующим в свертывании, является соль кальция. Если ее удалить из состава биологической жидкости, процесс протекать не будет.
Как проходит свертывание
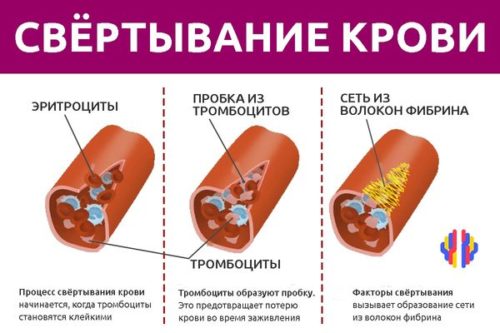 Процесс сводится к образованию тромбоцитарно-фибринового сгустка. Он образуется в несколько этапов. Изначально происходит краткосрочный первичный спазм сосудов. Потом за счет адгезии тромбоцитов формируется пробка. На завершающей стадии формирования обеспечивается процесс ретракции, заключающийся в сокращении и уплотнении пробки.
Процесс сводится к образованию тромбоцитарно-фибринового сгустка. Он образуется в несколько этапов. Изначально происходит краткосрочный первичный спазм сосудов. Потом за счет адгезии тромбоцитов формируется пробка. На завершающей стадии формирования обеспечивается процесс ретракции, заключающийся в сокращении и уплотнении пробки.
Сразу после повреждения сосудов усиливается работа тромбоцитов. Они прикрепляются к волокнам соединительных тканей по краям раны. Одновременно с адгезией происходит агрегация. Активированные тромбоциты присоединяются к повреждённым краям раны и создают формирования, препятствующие массивным кровопотерям. Появляется тромбоцитарная пробка.
После описанных процессов запускается активная секреция, усиливающая производство некоторых гормонов. Выделяется адреналин и норадреналин. Это приводит к необратимой агрегации. Совместно с освобождением перечисленных веществ образуется тромбин. Он действует на фибриноген, затрагивающий лейкоциты и эритроциты. Тромбоциты при помощи белка тромбосептина притягиваются друг к другу.
Эритроциты
Кровь имеет красную окраску благодаря эритроцитам. Они являются самыми многочисленными из форменных элементов. В зрелом состоянии эритроцит не содержит ядра. Срок их жизни, когда они циркулируют по организму — 120 дней, а затем они разрушаются в печени и селезенке. В состав эритроцитов входит железосодержащий белок — гемоглобин, благодаря которому обеспечивается основная функция эритроцитов — это транспорт кислорода и других газов. В легких человека гемоглобин связывает кислород, там он превращается в вещество светло-красного цвета оксигемоглобин. Далее, переходя в ткани, оксигемоглобин высвобождает кислород, образуется гемоглобин, кровь снова приобретает более насыщенный, темный оттенок. Карбогемоглобин из тканей в легкие переносит углекислый газ.
Чем опасно нарушение?
Кровь со сниженной способностью к свертываемости часто еще называют «жидкой». Это связано с тем, что она «более текучая», в результате чего кровотечение даже из небольших ранок может долго не останавливаться.
READ Покажет ли рак общий анализ крови при онкологии?
Так, люди с пониженной способностью к коагуляции входят в группу риска и могут пострадать от значительной кровопотери из-за ран, которые для человека с нормальной свертываемостью не опасны.
Различают 3 степени тяжести кровопотери:
Значительная кровопотеря может привести к летальному исходу.
К пациентам с пониженной свертываемостью крови обычно относятся более внимательно, учитывая возможные риски.
У таких людей период реабилитации после различных травм (или операций) длится дольше, а хронические заболевания протекают тяжелее.
Видео:
Возникновение кровотечений вследствие воспалений внутренних органов для таких людей намного опаснее, чем для тех, у кого процессы коагуляции протекают нормально.
Плохая свертываемость крови при беременности грозит ранней отслойкой плаценты и возможными осложнениями во время и после родов.
Нередко у женщин и мужчин с «жидкой кровью» отмечается склонность к пониженному давлению, повышается опасность кровоизлияния в мозг и возникают частые кровотечения из носа.
Плохая свертываемость крови у ребенка может сказаться и на иммунитете, подрывая защитные функции организма и делая малыша более уязвимым перед различными заболеваниями.
READ Возрастные нормы гемоглобина у мужчин
Гемостаз в организме женщины
Отдельного внимания заслуживает гемостаз в организме женщины. Женский организм — очень тонкий инструмент. Факторов, влияющих на гемостаз, достаточно: окружающая среда, питание, физические нагрузки, хронические заболевания, а так же факторы, которые характерны только для женщин: ежемесячное колебание гормонального фона, вызванное менструальным циклом, прием гормональной контрацепции, беременность, роды.
Гормональная терапия, контрацептивны, ЭКО
Одним из эффектов такой терапии является увеличение концентрации фибриногена (независимый фактор сосудистого риска), увеличение синтеза в печени витаминов, так называемых К-зависимых факторов свертывания крови (II, VII, IX, X), которые снижают концентрацию антитромбина III.
Все это может привести к серьезному увеличению риска тромбообразования (гиперкоагуляция). Именно поэтому в противопоказаниях для гормонального лечения находится повышенная свертываемость крови.
Исследования системы гемостаза необходимо проводить при назначении врачом заместительной гормональной терапии в период менопаузы, при назначении гормональной стимуляции при ЭКО, а так же при подборе гормональных контрацептивов.
Беременность и роды
Актуальность исследования состояния гемостаза у беременных, рожениц и женщин послеродового периода неоспорима. В определенной степени это объясняется рядом физиологических особенностей: сдавление беременной маткой нижней полой и подвздошных вен, увеличение объема циркулирующей крови.
С первых дней беременности в результате работы «гормонов беременности» происходит значительная перестройка свертывающей системы, резко увеличивается способность образовывать тромбы, тем самым подготавливая женщину к процессу родов.
Во время беременности система гемостаза влияет на развитие плода следующим образом: через плаценту от матери к ребенку поступают все необходимые питательные вещества и кислород, от качества кровотока зависит рост и развитие, если гемостаз матери имеет отклонения от нормы, то есть риск нарушения развития плода. Также нарушение гемостаза при вынашивании беременности может нести негативные последствия и для самой матери, чреватое образование тромбоза либо кровотечением.
Исследовать систему гемостаза нужно ещё на этапе планирования беременности, чтобы при необходимости пройти курс профилактической терапии
Это особенно важно, если вы входите в «группу риска»: у кого-то из ваших родственников был инсульт, инфаркт или тромбоз; ваша предыдущая беременность закончилась выкидышем или была замершей; вы занимаетесь спортом с тяжёлыми физическими нагрузками; у вас или у кого-то из кровных родственников (мамы или бабушки) варикозное расширение вен. Также рекомендуют сделать анализ на гемостаз женщинам, у которых предыдущая беременность сопровождалась тяжелым токсикозом, внутриутробной гибелью плода или задержкой его развития
Послеродовый период
Изменения в системе гемостаза, выявленные во время беременности, сохраняются еще в течение как минимум 6 месяцев, поэтому очень важно продолжать назначенную терапию, проходить наблюдение и исследование свертываемости крови, в соответствии с рекомендациями лечащего врача
Лечение
Терапия назначается только после полного обследования пациента и установления конкретной причины.
Если выяснена связь с лекарственными препаратами антикоагулянтного вида, то они отменяются. Через некоторый срок по повторным анализам судят об улучшении свертывающих свойств.
Лейкозы, анемии, болезни печени требуют специфического лечения. Только при устранении обострения основного заболевания можно поднять показатели свертываемости.
В качестве симптоматической терапии часто назначаются препараты кальция, викасол, фолиевая кислота.
Пациентам рекомендуется добавить к пищевым продуктам молочные изделия, творог, сыр (считается, что максимальное количество кальция в сыре сорта «Чеддер»), листья салата, лук, капусту, мясо и рыбу в достаточном количестве.
Как происходит свертывание крови?
Каждый человек хоть раз в жизни получал небольшую рану или царапину, в результате чего имел возможность понаблюдать за процессом превращения крови в сгусток. Данный процесс так и именуется – свертывание крови. Он является жизненно необходимым для всех живых организмов, имеющих жидкую внутреннюю среду организма. Запуск биохимических реакций обеспечивается благодаря наличию в крови специальных белков, которые называют факторами свертывания крови.
Сам процесс свертывания сложный и состоит из множества этапов. Примитивно его можно описать следующим образом:
- Ферментативное превращение растворимого белка плазмы фибриногена в полимер с помощью тромбина.
- Протеолитическое отщепление небольшого фрагмента пептидного фрагмента.
- Освобождение участков связывания, в результате чего молекула фибрина агрегирует в полимер.
- Образование изопептидных связей, боковых цепей аминокислот фибрина, в результате чего образуется нерастворимый фибриновый сгусток, тромб.
Белки, участвующие в свертывании крови
Свертывающая система крови функционирует благодаря протеканию совокупности последовательных биохимических реакций. Непосредственное участие в этом процессе принимают белки плазмы крови и ионы кальция, которые в совокупности названы факторами свертывания крови (ФСК). Их принято обозначать римскими цифрами:
- I — фибриноген;
- II — протромбин;
- III — тромбопластин;
- IV — кальций;
- V и VI — плазменный и сывороточный акцелераторы-глобулины;
- VII — конвертин;
- VIII — антигемофильный глобулин А;
- IX — антигемофильный глобулин В (т. н. Кристмас-фактор);
- Х — Стюарт — Проувер-фактор (аутопротромбин С, тромботропин);
- XI — плазменный предшественник тромбопластина;
- XII — фактор Хагемана;
- XIII — фибрин-стабилизирующий фактор (фибринолигаза).
Ряд названных компонентов содержится в форменных элементах крови. К примеру, тромбоциты имеют 3 фактора: предшественник тромбопластина, аналоги V и XIII факторов, фибриногена. Среди ведущих реакций свертывания крови с протеканием ферментов можно выделить:
- Образование активного тромбопластина.
- Превращение протромбина в тромбин.
- Превращение фибриногена в фибрин.
Этапы свертывания крови
Сам процесс свертывания крови длится всего несколько минут. Однако он не происходит одномоментно и имеет свои определенные этапы, которые принято обозначать как фазы гемокоагуляции. Всего механизм свертывания крови насчитывается 4 такие стадии:
- Первая фаза – сокращение поврежденного сосуда. Необходимо для уменьшения кровообращения дистальной от травмированного участка области.
- Вторая фаза – образование рыхлой тромбоцитарной пробки в месте повреждения (белый тромб). Имеющийся коллаген становится связующим звеном для тромбоцитов. У данных клеток в результате связывания разрушается структура и происходит высвобождение тромбоксана и ADP. Они способствуют присоединению новых кровяных пластинок, в результате чего формируется рыхлая временная пробка.
- Третья фаза – формирование красного тромба (кровяного сгустка).
- Четвертая фаза – частичное или полное растворение сгустка.
С момента образования сгустка наступает послефаза. В норме послефаза гемокоагуляции включает в себя 2 параллельных процесса: ретракцию (сокращение, уплотнение) и фибринолиз (растворение) сгустка
Таким методом система крови предотвращает избыточное образование кровяных сгустков, что важно для предупреждения развития тромбоэмболии
Что влияет на свертываемость крови?
При развитии кровотечения активизируются факторы свертывания крови, сужаются сосуды, образуется тромб и кровопотеря превращается. При этом чрезмерного тромбообразования не происходит, так как вместе с системой, которая обеспечивает свертываемость крови, работает и другая – противосвертывающая система (фибринолиз). Изменение определенных факторов способно нарушить равновесие между ними, что приводит к тяжелым последствиям:
- повышение свертываемости крови ведет к тромбозам и эмболиям;
- снижение свертывания вызывает кровотечения.
В зависимости от того, как необходимо повлиять на процесс свертывания крови, фармакологические средства, используемые с этой целью, подразделяют на:
1. Средства, способствующие остановке кровотечения (гемостатики):
- коагулянты;
- ингибиторы фибринолиза, антагонисты гепарина.
2. Средства, препятствующие гемокоагуляции (антитромбические):
- антикоагулянты;
- активаторы фибринолиза;
- ингибиторы агрегации тромбоцитов (антиагреганты).
Какие показатели определяет анализ
- Время свертываемости и длительность кровотечения (ВСК и ДК) – временной период, за который оно останавливается после прокола кожи.
- АЧТВ – активированное частичное тромбопластиновое и тромбиновое время. Анализ показывает период, в течение которого образуется сгусток после добавления специальных реактивов. С помощью такого исследования имитируется каскад процессов, возникающих при гемостазе.
- Протромбиновое время и протромбиновый индекс и МНО (международное нормализованное отношение) – определяемые и высчитываемые показатели адекватности свертываемости.
- Концентрацию фибриногена – белка, участвующего в формировании сгустка.
- Количество тромбоцитов – кровяных телец, формирующих тромб.
Понижение этих показателей грозит кровопотерей даже при небольших повреждениях, а повышение указывает на склонность к тромбозам. Результаты сверх нормы наблюдаются при ДВС-синдроме – внутрисосудистом свертывании, сопровождающем травмы, обширные гнойные процессы, укусы змей, отравления, инфекции, лейкозы, тяжелую недостаточность внутренних органов.
- Волчаночный коагулянт образуется при неправильной работе иммунной системы, которая начинает тормозить образование тромбов, приводя к кровотечениям. В норме этого вещества в анализе быть не должно.
- Антитромбин III – белок, замедляющий образование кровяного сгустка и тормозящий активность веществ-коагулянтов.
- D-димер – маркер тромбозов. Это вещество остаётся после разрушения фибриногена, находящегося в тромбе. Поскольку организм старается разрушить мешающие сгустки, рост концентрации D-димера свидетельствует об обширном тромбозе.
Уменьшение концентрации противосвертывающих компонентов приводит к образованию тромбов в ногах, сердечных сосудах, головном мозге, внутренних органах. У женщин такое нарушение приводит к выкидышам из-за тромбоза плацентарных сосудов. Это состояние часто бывает наследственным, но может вызываться и различными заболеваниями.
| Показатель свертываемости | Норма | Причины увеличения | Причины уменьшения |
| Время свертываемости | 5-7 мин | Пониженное количество тромбоцитов (тромбоцитопения), дефицит факторов свертывания, лейкоз, анемия, цирроз печени, недостаток витамина К | Заболевания сердца и сосудов, ревматизм, гормональные нарушения, инфекции, отравления, повышенная выработка тромбоцитов, болезнь Виллебранда, Кристмаса, гемофилия |
| Длительность кровотечения | 5 мин | ||
| Тромбоциты | 180-320 х 10^9/л | Злокачественные новообразования в костном мозге, травмы, туберкулез, удаленная селезенка, ревматизм, колиты, почечная недостаточность | Снижение активности костного мозга, тромбоцитопеническая пурпура – заболевания, сопровождающиеся кровоизлияниями на коже и слизистых |
| АЧТВ | 21,1-36,5 сек. |
Болезнь Виллебранда, Кристмаса, гемофилия,
тяжелые болезни печени, дефицит витамина К, ревматические поражения, имеющийся волчаночный коагулянт |
Наследственная склонность к тромбозам, использование противозачаточных таблеток |
| Протромбиновое время | 11-15 с. | Наследственные нарушения свертываемости, дефицит фибрина и фибриногена, болезни печени и почек, нехватка витамина К, повышение антитромбина III | Первый триместр беременности, опухоли, некоторые типы лейкозов |
| Протромбиновый индекс | 72-123 % | ||
| Тромбиновое время | 14-21 сек. | Цирроз, гепатит, болезни почек, увеличение концентрации эритроцитов | Превышение количества тромбоцитов |
| Фибриноген | 1,8-3,5 г/л | Злокачественные опухоли, инфаркт, ожоги, перенесенные операции, туберкулез, грипп, недостаточность щитовидной железы, перенесенный инсульт, болезни легких | Гепатит, миелолейкоз, цирроз печени, нехватка витаминов, отравления |
| Антитромбин III | 66-124 % | Болезни печени и почек, тромбозы, операции, кровопотери, онкологические патологии | |
| Волчаночный коагулянт | Отсутствует | Волчанка, ревматизм, нарушения работы иммунной системы, колит, злокачественные опухоли | |
| D-димер | 248 нг/мл | Ревматоидный артрит, сердечно-сосудистые заболевания, тромбозы, болезни печени | – |