Иммунный ответ
Содержание:
- 27 Вопрос. Цитотоксический иммунный ответ
- Сила иммунного ответа
- Что такое иммунограмма?
- Нормальные показатели
- Как регулируется иммунный ответ?
- Формы иммунного ответа.
- Особые участки
- Иммунитет: зачем он нужен?
- Схема Th1 ответа. Эффекторы клеточного ответа.
- Стерильность: актуально ли?
- Общая информация
- Ифа, иммуноблоттинг. Компоненты, механизм, способы постановки, учетные признаки. Практическое применение
27 Вопрос. Цитотоксический иммунный ответ
Т-киллеры.
Убивают клетки-мишени, несущие чужеродные
или видоизменённые аутоантигены. В
большинстве случаев функция ЦТЛ также
МНС-рестригирована — цитотоксические
Т-лимфоциты распознаёт Аг в комплексе
с молекулой МНС I на мембране клетки-мишени.
Индукция цитотоксических свойств
клетки-предшественницы Т-киллера
происходит под действием двух сигналов.
Первый сигнал включает взаимодействие
между Т-киллером и МНС I на клетке-мишени.
Второй сигнал — ИЛ. Т-хелпер играет
ключевую роль в стимуляции цитотоксических
Т-лимфоцитов. Цитотоксический эффект
Т-киллеров реализуется через образование
в клетках-мишенях пор под действием
особых белков — перфоринов. Нарушение
осмотического баланса с внеклеточной
средой приводит к гибели клетки.
В
отличие от NK-клеток,
T-киллеры специфически распознают
определённыйантиген и
убивают только клетки с этим антигеном.
Нормальные
киллеры или NK
. Эти
клетки были названными естественными
киллерами, поскольку, по ранним
представлениям, они не требовали
активации для уничтожения клеток, не
несущих маркеров главного
комплекса гистосовместимости I
типа.
Основная
функция NK — уничтожение клеток организма,
не несущих на своей поверхности MHC1
и таким образом недоступных для действия
основного компонента противовирусного
иммунитета — Т-киллеров.
Уменьшение количества MHC1 на поверхности
клетки может быть следствием трансформации
клетки в раковую или действием вирусов,
таких как папилломавирус и ВИЧ.
NK
являются цитотоксичными; в их цитоплазме
находятся маленькие гранулы, содержащие
перфорин и протеазы.
Перфорин выделяется непосредственно
возле инфицированной клетки и образует
поры в её клеточной мембране, через
которые заходят протеазы и другие
молекулы, приводя к апоптозу или
осмотическому лизису клетки. Выбор
между апоптозом и лизисом имеет большое
значение, поскольку при лизисе зараженной
вирусом клетки произойдет освобождение
вирионов, а апоптоз приведет к разрушению
вирусов вместе с клеткой.
Сила иммунного ответа
Сила иммунного ответа зависит от способности организма реагировать на попадание инфекции, токсинов или ядов. Поэтому, в зависимости от силы, различают несколько видов иммунного ответа: нормоэргический, гипоэргический и гиперэргический.
Нормоэргический ответ – это соответствие силы иммунитета силе агрессии вредных микроорганизмов с последующим устранением последних. При данном типе иммунного ответа нарушение целостности тканей в процессе воспаления умеренное и не приводит к серьезным последствиям для организма. Нормоэргический иммунный ответ присущ людям с нормальной функцией иммунной системы.
Гипоэргический ответ – когда агрессия со стороны микроорганизмов сильнее иммунитета больного. В итоге организм не в состоянии полностью ограничить размножение инфекции, что переводит заболевание в хроническое состояние. Такая форма иммунного ответа характерна для людей детского и пожилого возраста, а также для лиц с первичным и вторичным иммунодефицитами.
Гиперэргический ответ формируется на фоне сенсибилизации организма по отношению к поступившему антигену, в несколько раз превышая силу агрессии микроорганизмов. В процессе гиперэргического иммунного ответа воспалительная реакция увеличивается до такого состояния, которое может повредить здоровые тканей организма. Возникновение данного типа иммунной реакции определяется особенностями микроорганизмов, а также индивидуальными показателями самой иммунной системы организма.
Гиперэргический иммунный ответ является основой формирования аллергической реакции.
Что такое иммунограмма?
Это специальный анализ крови, который позволяет оценить количество различных иммунных клеток, вырабатываемых ими антител и ряда других веществ, свидетельствующих о состоянии защитных систем организма. В зависимости от цели исследования и возможностей лаборатории, количество исследуемых параметров может существенно варьироваться. Расширенное исследование позволяет изучить более 25 различных показателей – такой анализ выявляет даже скрытые нарушения, которые невозможно обнаружить стандартными методиками.
Иммунитет человека можно условно разделить на два звена – «медленное» (гуморальное) и «быстрое» (клеточное). Быстрое звено реагирует практически сразу после попадания возбудителя болезни (вируса, гриба, бактерии, простейших и т.д.) в организм. В задачу этой группы клеток входят следующие функции:
- Поглотить и «переварить» вредоносного агента;
- Презентировать или «рассказать» о патогенном микроорганизме другим иммунным клеткам, которые не могут самостоятельно его обнаружить;
- Уничтожить наибольшее количество выявленных микробов;
- Бороться с различными опухолями и аутоиммунными процессами – еще одна важная функция иммунитета, которая часто не позволяет организму самостоятельно справиться с болезнью.
После того, как «быстрое» звено поглотило чужеродное тело и рассказало о нем «медленному» звену, запускается медленный процесс создания и выброса антител в кровь. Антитела – это вещества, уничтожающие определенный вид патогенного агента. Они очень специфичны и, в большинстве случаев, помогают организму окончательно справиться с имеющимся заболеванием. В среднем, продолжительность их создания составляет 2-3 недели.
Показатели иммунограммы отражают работу каждого из звеньев защиты. Именно на основании их изменений делается вывод об отсутствии/наличии иммунодефициты, о варианте нарушения и оптимальном методе терапии.
| Звено иммунитета, исследуемый параметр | Функция |
| Цитотоксические Т-клетки (CD3+, CD8+) | Распознавание вредоносных микроорганизмов и их уничтожение |
| Т-хелперы (CD4+) | «Рассказывают» о наличии патогена другим клеткам-защитникам, играют существенную роль в формировании длительного иммунитета. |
| Т-супрессоры (CD8+) | Регуляция активности защитных систем, предохраняют организм от развития аутоиммунных реакций (когда вырабатываются антитела против здоровых тканей) |
| Т-клетки с рецептором для ИЛ-2 (CD25+) | |
| Носители маркера апоптоза (CD95+) | Контроль скорости процесса самоуничтожения клеток |
| В-клетки (CD+, 19CD+) | Отвечают за выработку специфических антител. В большинстве случаев, именно благодаря данному пулу клеток происходит полное выздоровление.
Защищают организм от повторного заражения той же самой инфекцией, в течение определенного времени. |
| Иммуноглобулин G | Антитела, вырабатываемые В-клетками. При связывании с вредоносным микробом – разрушают его стенку, вследствие чего наступает гибель. |
| Иммуноглобулин M | |
| Иммуноглобулин A | |
| Иммуноглобулин | Отвечает за развитие любых аллергических реакций. |
| стественные/натуральные киллеры (CD16+) или NK-клетки | Обеспечивают естественный противоопухолевый иммунитет |
| Клетки с HLA маркером | Отражает активность работы иммунных механизмов |
| Фагоцитоз | Распознавание, поглощение и презентация Т-клеткам вредоносных агентов |
| Реакция торможения миграции лейкоцитов (сокращенно – РТМЛ) | Лабораторный тест, отражающий работу клеточного звена. |
| НСТ-тест | Позволяет оценить активность фагоцитоза |
| Комплемент | Предотвращает формирование больших по размеру иммунных комплексов (соединений вредоносных частиц с антителами). Участвует в нейтрализации микробов |
В некоторых случаях, доктор может порекомендовать дополнить анализ исследованием содержания интерлейкинов в крови – это специальные вещества, которые обеспечивают взаимосвязь различных компонентов защитных систем. При нарушении их выработки также могут формироваться иммунодефицитные состояния.
Нормальные показатели
Если у пациента повышен ИРИ, то это может быть признаком серьезных заболеваний. Однако невозможно поставить диагноз только лишь по данным иммунограммы. В данном случае необходимо пройти дополнительное обследование. При аутоиммунных патологиях больному показан длительный прием кортикостероидов и иммуносупрессоров, а также диспансерное наблюдение.
Что делать, если ИРИ снижен? Такой показатель является признаком ослабления защитных сил организма. Существуют ли препараты для повышения иммунорегуляторного индекса? Если снижение ИРИ спровоцировано инфекционной патологией или хроническими болезнями, то иммунитет самостоятельно приходит в норму после выздоровления или достижения ремиссии. В некоторых случаях пациентам назначают иммуномодуляторы:
- «Виферон»;
- «Полиоксидоний»;
- «Арбидол»;
- «Иммунал»;
- «Циклоферон».
Однако такие препараты можно принимать только по назначению и под контролем врача. Со временем организм привыкает к иммуномодуляторам, и эффективность таких лекарств уменьшается. Злоупотребление иммуностимулирующими препаратами может привести к истощению собственной иммунной системы.
Увеличение IgA происходит при хронических болезнях печени, аутоиммунных заболеваниях, миеломе, гломерулонефрите, алкогольной интоксикации. Снижению концентрации иммуноглобулина А способствуют физиологические изменения у ребенка до 6 месяцев, циррозное поражение печени, лучевая болезнь, терапия иммунодепрессантами, отравление организма химическими веществами.
Рост содержания IgG отмечается при аутоиммунных заболеваниях, миеломе, ВИЧ-инфекции, мононуклеозе инфекционной этиологии, инфекционных патологиях. Снижение иммуноглобулина G происходит в результате физиологических изменений у ребенка в возрасте до 6 месяцев, лучевой болезни, отравления химическими веществами, терапии иммунодепрессантами.
Антинуклеарные антитела повышаются при аутоиммунных патологиях, нефрите, хроническом гепатите, васкулите. Показатель АСЛО растет при острой форме гломерулонефрите, ревматизме, рожистом воспалении, скарлатине и инфицировании стрептококками. Антиспермальные антитела повышены при риске бесплодия. Показатель MAR-теста увеличен при вероятном бесплодии мужчины. Показатели АТ-ТГ и АТ-ТПО увеличиваются при аутоиммунном тиреоидите, болезни Грейвса, синдроме Дауна и Тернера.
Анализ на ЦИК (циркулирующие иммунные комплексы) назначают при: обследовании на наличие аутоиммунных патологий и дефицита комплемента, иммунопатогенетических поражениях почек, артритах различной этиологии, персистирующей инфекции. Циркулирующие иммунные комплексы повышены при остром инфицировании организма, персистирующей инфекции, аутоиммунных патологиях, аллергическом альвеолите, гломерулонефрите в острой форме, местной анафилаксии, сывороточной болезни, эндокардите, злокачественных опухолях, болезни Крона. Также циркулирующие иммунные комплексы исследуют в рамках общего иммунологического обследования.
Как регулируется иммунный ответ?
Защитная система организма отличается множеством механизмов контроля и регуляции протекающих в ней реакций. Это жизненно необходимо для любого сложного организма, так как если иммунный ответ будет слишком сильным – возникнут аутоиммунные заболевания и аллергии. При слишком слабой реакции – организм может не справиться с инфекцией либо ядом и получить фатальные повреждения.
Регуляция осуществляется на трех уровнях:
- Саморегуляция за счет внутренних механизмов взаимодействия иммунных клеток;
- Влияние гормональной системы и печени;
- Воздействие нервной системы.
Для саморегуляции в иммунной системе присутствуют специальные Т-хелперы, которые способны активировать либо подавлять производство антител. Также существуют особые клетки, которые производят антиидиотипы – особые белки связывающие собственные антитела, выработанные организмом ранее. Они нужны для своевременного снижения их концентрации, когда необходимость в большом количестве специфических иммуноглобулинов пропадает.
Гормональная система также играет большую роль в регуляции механизмов иммунного ответа. Практически все гормоны обладают способностью подавлять либо усиливать иммунные реакции. Например, гормон надпочечников гидрокортизон обладает мощным подавляющим действием на иммунный ответ. Поэтому препараты на его основе часто применяют для лечения аутоиммунных заболеваний.
Хорошим примером гормона – стимулятора иммунной системы является мелатонин (вырабатывается в шишковидной железе). Он оказывает мощное стимулирующее действие на иммунитет, но механизм его воздействия точно не установлен.

Печень является центром выработки различных иммуносупрессивных соединений. Играет важную роль в остановке активной фазы иммунного ответа, снижении активности лимфоцитов и макрофагов.
Активная роль центральной нервной системы в регуляции иммунного ответа давно известна. Осуществляют ее глубинные участки головного мозга, связанные с лимбической системой и отвечающие за психоэмоциональное состояние человека. Достоверно установлено, что депрессии и другие психические нарушения способны серьезно снижать активность защитной системы организма. Механизм регуляторного воздействия основан на передаче сигналов от нейронов непосредственно к клеткам иммунной системы.
Во многом параметры регуляции иммунной системы закладываются на генном уровне. У каждого человека закладывается индивидуальный набор генов, экспрессия которых в Т-хелперах обуславливает разную силу ответа у каждого индивидуума. За счет этого глубокого уровня регуляции природа создает большое разнообразие защитных реакций, что усложняет распространение инфекций в популяции.
Формы иммунного ответа.
Иммунный ответ – это цепь последовательных сложных кооперативных процессов, идущих в иммунной системе в ответ на действие антигена в организме.
Различают:
1) первичный иммунный ответ (возникает при первой встрече с антигеном);
2) вторичный иммунный ответ (возникает при повторной встрече с антигеном).
Любой иммунный ответ состоит из двух фаз:
1) индуктивной; представление и распознавание антигена. Возникает сложная кооперация клеток с последующей пролиферацией и дифференцировкой;
2) продуктивной; обнаруживаются продукты иммунного ответа.
При первичном иммунном ответе индуктивная фаза может длиться неделю, при вторичном – до 3 дней за счет клеток памяти.
В иммунном ответе антигены, попавшие в организм, взаимодействуют с антигенпредставляющими клетками (макрофагами), которые экспрессируют антигенные детерминанты на поверхности клетки и доставляют информацию об антигене в периферические органы иммунной системы, где происходит стимуляция Т-хелперов.
Далее иммунный ответ возможен в виде по одного из трех вариантов:
1) клеточный иммунный ответ;
2) гуморальный иммунный ответ;
3) иммунологическая толерантность.
Клеточный иммунный ответ – это функция Т-лимфоцитов. Происходит образование эффекторных клеток – Т-киллеров, способных уничтожать клетки, имеющие антигенную структуру путем прямой цитотоксичности и путем синтеза лимфокинов, которые участвуют в процессах взаимодействия клеток (макрофагов, Т-клеток, В-клеток) при иммунном ответе. В регуляции иммунного ответа участвуют два подтипа Т-клеток: Т-хелперы усиливают иммунный ответ, Т-супрессоры оказывают противоположное влияние.
Гуморальный иммунитет – это функция В-клеток. Т-хелперы, получившие антигенную информацию, передают ее В-лимфоцитам. В-лимфоциты формируют клон антителопродуцирующих клеток. При этом происходит преобразование В-клеток в плазматические клетки, секретирующие иммуноглобулины (антитела), которые имеют специфическую активность против внедрившегося антигена.
Образующиеся антитела вступают во взаимодействие с антигеном с образованием комплекса АГ – АТ, который запускает в действие неспецифические механизмы защитной реакции. Эти комплексы активируют систему комплемента. Взаимодействие комплекса АГ – АТ с тучными клетками приводит к дегрануляции и выделению медиаторов воспаления – гистамина и серотонина.
При низкой дозе антигена развивается иммунологическая толерантность. При этом антиген распознается, но в результате этого не происходит ни продукции клеток, ни развития гуморального иммунного ответа.
Иммунный ответ характеризуется:
1) специфичностью (реактивность направлена только на определенный агент, который называется антигеном);
2) потенцированием (способностью производить усиленный ответ при постоянном поступлении в организм одного и того же антигена);
3) иммунологической памятью (способностью распознавать и производить усиленный ответ против того же самого антигена при повторном его попадании в организм, даже если первое и последующие попадания происходят через большие промежутки времени).
Особые участки
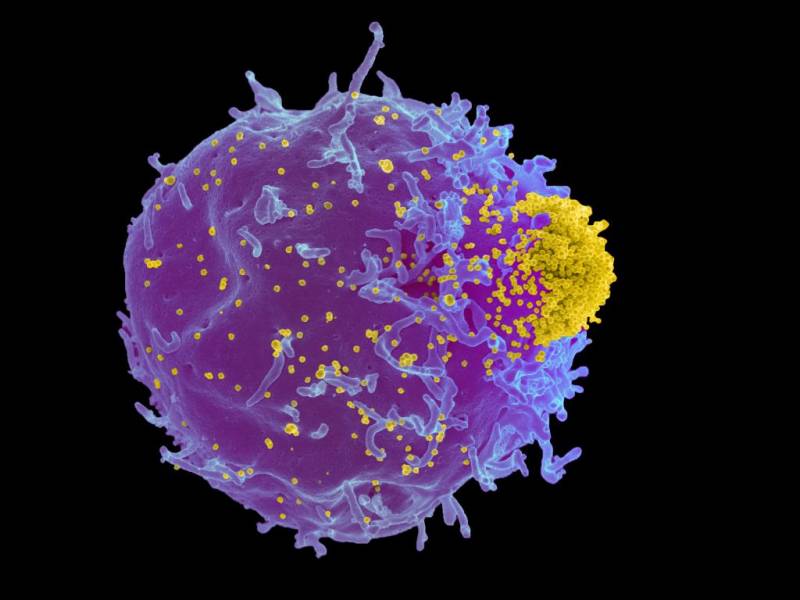
Иммунологи Центра гематологии также описали участки спайк-белка SARS-CoV-2, которые вызывают наиболее сильный иммунный ответ у переболевших COVID-19. Встретившись с этим белком, защитная система человека «запоминает» вирус, и, если он попадет в организм, сможет его обезвредить.
Тело без антитела
Фото: ИЗВЕСТИЯ/Зураб Джавахадзе
Оказалось, что два участка вируса распознаются иммунной системой большинства людей-носителей самого распространенного в Европе варианта гена HLA-A, отвечающего за демонстрацию фрагментов вирусов Т-лимфоцитам. Оба выявленных фрагмента уникальны для нового SARS-CoV-2, то есть отличают его от других коронавирусов. Значит, их можно использовать, чтобы выделять людей, переболевших именно COVID-19.
— Нужно понимать, что Т-лимфоциты распознают вирус не целиком, а его короткие фрагменты. И у разных людей в силу генетических особенностей эти фрагменты разные, — сообщил «Известиям» заведующий лабораторией трансплантационной иммунологии в НМИЦ гематологии Минздрава России Григорий Ефимов. — Выходит, что вирусу не так просто уйти от иммунной системы, ведь он мог бы внести мутации в распознаваемые участки и тем самым стать невидимым для Т-лимфоцитов. Но это сложно, так как такие мутации против одного человека будут эффективны, а для других нет.
Понимание того, какие именно фрагменты вируса распознает иммунитет большинства людей, поможет определить, насколько эффективны вакцины и содержат ли они именно эти уникальные участки. Также это позволит создать максимально эффективные тест-системы, которые будут показывать уровень Т-лимфоцитов, и указывать именно на SARS-CoV-2, а не какой-либо другой коронавирус.
Иммунитет: зачем он нужен?
Иммунная система отвечает за антигенный гомеостаз. В принятой в науке терминологии иммунитетом именуют невосприимчивость к определенному типу патологических микроскопических форм жизни и продуктов их жизнедеятельности, а также ядов, генерируемых животным. Иммунная система принимает участие в опознании и деструкции самых разных клеточных структур – бактерий и вирусов, паразитарных, простейших, грибковых, опухолевых. Иммунный ответ, возникающий при этом – это реакция на инвазию.
Эволюция – особенность, присущая любой форме жизни, но особенно ярко она прослеживается, если наблюдать за микроорганизмами. Свойства микроскопических форм жизни постоянно совершенствуются, и единственным эффективным ответом на это со стороны макроорганизмов оказалось формирование иммунитета разных видов. Впрочем, иммунитет не единственное, что защищает человека. Немалую роль играют факторы, не допускающие инвазию. К примеру, проникновение патологической микрофлоры в человеческий организм затруднено за счет эпителиальных ресничек, кожных покровов, слизистых, а также высокой кислотности желудочной среды.
Схема Th1 ответа. Эффекторы клеточного ответа.
Пусковым звеном в формировании клеточного
типа иммунного ответа является продукция
макрофагом, на территории которого идет
процессинг антигена, интерлейкина
ИЛ-12. События развиваются следующим
образом.
ГКГС — I макрофага презентирует пептид
(антиген) Т-хелперу (CD 4 ). Под влиянием
ИЛ-12, продуцируемого этим же макрофагом,
Th трансформируется в Th 1. g — IFN является
важнейшим из цитокинов , выделяемых Th
1. Он активирует контакт Т CD 8 с рецептором
ГКГС — I макрофага, на котором представлен
тот же антиген. Выделяемый Th 1 ИЛ-2
стимулирует пролиферацию таких, уже
антигенспецифических Т-цитолитических
лимфоцитов (Тс). Главной функцией Т с в
противоинфекционной защите является
уничтожение соматических клеток
организма, внутри которых находится
возбудитель, а на поверхности — метка,
комплекс ГКГС-I — антиген патогена . При
прямом контакте с такой клеткой Т с
выделят гранулы, содержащие белки —
перфорин , гранзим . Перфорин встраивается
в мембрану соматической клетки, образует
в ней каналы «поры» и может действовать
как мембраноатакующий белок. Гранзим
( сериновые протеиназы ) индуцирует один
из вариантов апоптоза и гибель соматической
клетки вместе с находящимися в ней
микробами.
Выделяют три основные группы Т- лимфоцитов-
помощники (активаторы), эффекторы,
регуляторы.
Первая группа- помощники (активаторы),
в состав которых входят Т- хелперы1, Т-
хелперы2, индукторы Т- хелперов, индукторы
Т- супрессоров.
1. Т- хелперы1 несут рецепторы CD4 (как и
Т- хелперы2) и CD44, отвечают за созревание
Т- цитотоксических лимфоцитов (Т-
киллеров), активируют Т- хелперы2 и
цитотоксическую функцию макрофагов,
секретируют ИЛ-2, ИЛ-3 и другие цитокины.
2. Т- хелперы2 имеют общий для хелперов
CD4 и специфический CD28 рецепторы,
обеспечивают пролиферацию и дифференцировку
В- лимфоцитов в антителпродуцирующие
(плазматические) клетки, синтез антител,
тормозят функцию Т- хелперов1, секретируют
ИЛ-4, ИЛ-5 и ИЛ-6.
3. Индукторы Т- хелперов несут CD29, отвечают
за экспрессию антигенов HLA класса 2 на
макрофагах и других А- клетках.
4. Индукторы Т- супрессоров несут CD45
специфический рецептор, отвечают за
секрецию ИЛ-1 макрофагами, активацию
дифференцировки предшественников Т-
супрессоров.
Вторая группа- Т- эффекторы. В нее входит
только одна субпопуляция.
5. Т- цитотоксические лимфоциты (Т-
киллеры). Имеют специфический рецептор
CD8, лизируют клетки- мишени, несущие
чужеродные антигены или измененные
аутоантигены (трансплантант, опухоль,
вирус и др.). ЦТЛ распознают чужеродный
эпитоп вирусного или опухолевого
антигена в комплексе с молекулой класса
1 HLA в плазматической мембране клетки—
мишени.
Третья группа- Т-клетки- регуляторы.
Представлена двумя основными
субпопуляциями.
6
Т- супрессоры имеют важное значение
в регуляции иммунитета, обеспечивая
подавление функций Т- хелперов 1 и 2, В-
лимфоцитов. Имеют рецепторы CD11, CD8
Группа
функционально разнородна. Их активация
происходит в результате непосредственной
стимуляции антигеном без существенного
участия главной системы гистосовместимости.
7. Т- контсупрессоры. Не имеют CD4, CD8, имеют
рецептор к особому лейкину. Способствуют
подавлению функций Т- супрессоров,
вырабатывают резистентность Т- хелперов
к эффекту Т- супрессоров.
Стерильность: актуально ли?
Выделяют стерильный иммунитет и не являющийся таковым. Стойкость к возбудителям заболеваний формируется, если человек перенес инфицирование. В ходе ответа организма основной процент патологических форм жизни уничтожается, но не всегда микробы выводятся бесследно. В ряде случаев некоторое количество сохраняется в организме. Таким возбудителям не свойственно размножение, агрессия. Состояние называют нестерильным иммунитетом, обеспечиваемым невысокой концентрацией возбудителя в человеческом организме. Этот случай сопряжен с опасностью рецидива, если иммунитет ослабевает. Локализовать, победить болезнь обычно довольно просто, поскольку внутренние системы на клеточном уровне знают, как бороться с проблемой.
Стерильный иммунитет – такое состояние, когда возбудитель устраняется бесследно. Он формируется при получении вакцины. Такой появляется, например, если человек переболеет гепатитом А на фоне заражения вирусом.
Общая информация
Иммунный ответ – это последовательность непростых биологических процессов, протекающих в иммунной системе. Их задача – отреагировать на опасный антиген. Реакция возможна первичная, формирующаяся, когда антиген оказывается в теле человека впервые, вторичная – появляющаяся при повторении ситуации.
Первая фаза реакции индуктивна, макроорганизм опознает антиген. На клеточном уровне происходит координация ресурсов, затем клетки активно размножаются и дифференцируются. Следующий этап начинается, когда клетки иммунного ответа проявляют активность относительно вредоносных структур. Анализы помогают определить результаты реакции ответа.
Ифа, иммуноблоттинг. Компоненты, механизм, способы постановки, учетные признаки. Практическое применение
Метод
основан на использовании в качестве
метки антител ферментов, способных
разлагать субстрат и приводить к
образованию окрашенного продукта
(хромогена). Конъюгированные с ферментом
Ат сохраняют способность соединяться
с гомологичным АГ. Интенсивность окраски
соответствует количеству комплексов
АГ-АТ-фермент.
Определение
неизвестных АТ:
1)
фиксация известного АГ
2)
внесение неизвестной сыворотки
3)
внесение конъюгата (АТ + фермент)
4)
инкубация с хромогенным субстратом
Определение
неизвестных АГ:
1)
фиксация известного АТ
2)
внесение АГ-содержащего материала
3)
внесение двух АТ той же специфичности
(зачем — не
знаю, в таблице этого не было)
4) внесение конъюгата
(антиглобулин + фермент)
5) инкубация с
хромогенным субстратом
Положительная
реакция (связывание) — коричневый
Отрицательная
— желтый
В
основе метода — твердофазный вариант
ИФА для обнаружения неизвестных АТ.
1.
Препарат известного АГ разделяют на
фракции при помощи электрофореза на
агарном геле
2.
Гельнакладывают на фильтр, плотно
прижимают и создают электрическое поле,
в результате чего происходит перенос
фракций на бумагу (блоттинг)
3.
Добавляют сыворотку крови больного
4.
Добавляют меченную сыворотку против
Yg человека. Она соединяется с образовавшимися
комплексами АГ-АТ.
5.
Добавляют субстрат (хромоген), который
вызывает окрашивание комплексов
АГ-АТ-меченная сыворотка.