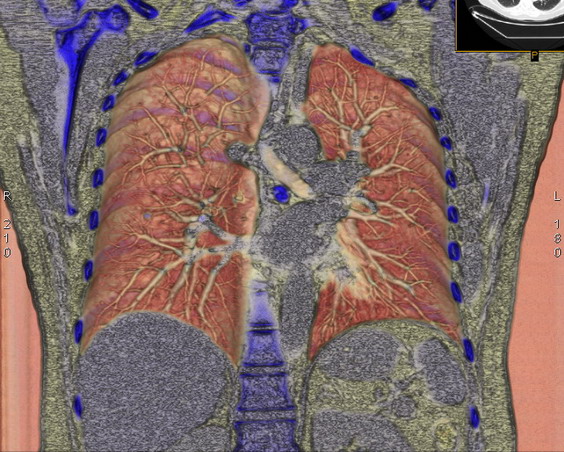
Интерстициальные заболевания лёгких
Содержание:
Особенности заболевания
Характеризуется патология хронической болевой симптоматикой в области таза, императивными (повелительными) позывами к мочеиспусканию, его учащения днем и в ночное время. Мужчины, дети и люди пожилого возраста менее подвержены интерстициальному циститу.
Основной контингент пациентов – женщины, переступившие 40-летний рубеж. Но, лишь малому количеству пациенток диагноз ставиться сразу (ввиду сложности диагностики). Обычно, с момента проявления характерной симптоматики до установления правильного диагноза проходит не один год.
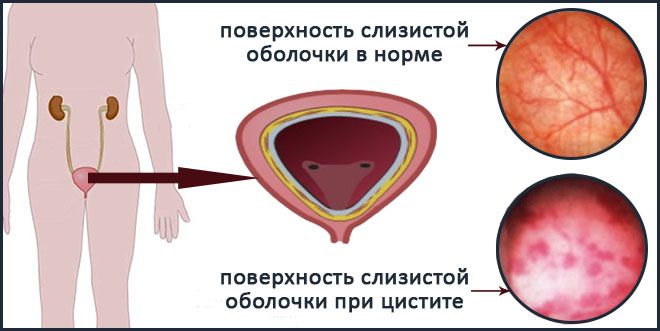 Фотографии слизистой оболочки мочевого пузыря в нормальном состоянии и при цистите, сделанные во время цистоскопии.
Фотографии слизистой оболочки мочевого пузыря в нормальном состоянии и при цистите, сделанные во время цистоскопии.
Это обусловлено тем, что при дополнительном диагностическом обследовании пациенток, какие-либо инфекционные процессы, новообразования или аномальное развитие моче пузырного органа не обнаруживаются, моча при этом – достаточно стерильна.
Лечение
Интерстициальный отёк лёгких – серьёзное заболевание, при котором пациенту показана интенсивная терапия. Все лечебные мероприятия проводятся только в условиях стационара под постоянным контролем врачей.
Лечение интерстициального отёка лёгких включает:
- применение кислородной маски;
- повышение артериального давления (при существенном его снижении);
- нормализацию сердечных сокращений;
- устранение болевого синдрома;
- внутривенное введение мочегонных препаратов;
- вливание пациенту плазмы крови (при пониженном уровне белка);
- приём глюкокортикостероидов (при бронхиальных спазмах);
- антибиотикотерапию (при выявлении в организме инфекции, например, сепсиса).
В зависимости от результатов комплексного обследования все мероприятия и препараты назначаются индивидуально, для каждого больного составляется своя схема лечения.
При быстрой постановке диагноза и своевременном принятии мер пациент, как правило, излечивается и его выписывают из стационара примерно через 3 недели.
Патогенез
Конечные отделы дыхательного тракта состоят из бронхиол (терминальных и респираторных), ацинусов и долек. Терминальные бронхиолы — воздухопроводящие, а респираторные участвуют в газообмене, поскольку через поры связаны с альвеолами. Ацинус — это структура легкого, где происходит газообмен, включает несколько респираторных бронхиол. Ацинусы (от 3 до 24) объединяются в легочные дольки. Каркас дольки включает междольковые перегородки, периартериальную, перибронхиальную соединительную ткань, соединительную ткань перегородок альвеол и ацинусов.
Соединительная ткань состоит из коллагеновых, ретикулярных и эластиновых волокон. Переплетения волокон коллагена и эластина имеются вокруг бронхов и в альвеолярных стенках, что обуславливает эластические свойства легких. Коллаген обеспечивает жесткость внутрилегочного каркаса.
Клетки соединительной ткани (гладкомышечные и фибробласты) синтезируют эластин и коллаген. Первостепенная роль его — поддержание тонуса терминальных отделов дыхательных путей. Одновременно клетки соединительной ткани синтезируют и ферменты (протеазы), ответственные за разрушение эластина и коллагена. Ферментная и антиферментная система в обычных условиях находятся в равновесии. В условиях инфекционного воспаления они продолжают оказывать эластолитическое (направленное на разрушение) действие за счет высокой продукции эластазы (фермент, разрушающий эластические волокна, эластин, коллаген). Это вызывает разрушение нормального соединительнотканного матрикса, происходит разрушение альвеолярных стенок и формируются общие полости. Избыточная продукция эластазы либо отсутствие ферментов для ее разрушения отмечается при ряде заболеваний легких (ХОБЛ, эмфизема, муковисцидоз).
Параллельно при воспалительных процессах отмечается активация фибробластов, которые продуцируют коллаген. В результате происходит усиленный процесс развития соединительной ткани в паренхиме легких и формирование фиброза. Развитию фиброзных изменений предшествует отек и инфильтрация легочной ткани. При разрушении мембраны альвеол на этом месте развивается внутриальвеолярный фиброз — разрастания соединительной ткани распространяются внутрь альвеол. Потом в патологический процесс вовлекается соединительная ткань вокруг артерий и бронхов.
В настоящее время более приемлемой теорией патогенеза силикоза и прочих пневмокониозов является иммунологическая, которая утверждает, что развитие данных профессиональных заболеваний невозможно без фагоцитоза пылевых частиц альвеолярными макрофагами. Скорость их гибели зависит от фиброгенной агрессивности пыли и пропорциональна ей. Гибель альвеолярных макрофагов — обязательный этап при образовании силикотического узелка. Формирование узелка возможно при условии многократно повторяющегося фагоцитирования пыли. Образующиеся провоспалительные медиаторы (цитокины) провоцируют накопление воспалительных клеток в перегородках альвеол, а кислородные радикалы, повреждая ткани легкого, вызывают гибель макрофагов.
Протеолитические ферменты (металлопротеиназа и эластаза) высвобождаются из разрушенных макрофагов и разрушают ткани легкого. Фаза воспаления сопровождается восстановительными процессами, при которых факторы роста стимулируют образование клеток, эпителия и новых сосудов в поврежденных тканях. Неконтролируемые процессы эпителизации приводят к развитию фиброза. Одно из ключевых значений в фиброгенезе имеют факторы роста. Доказано их стимулирующее действие на разрастание фибробластов и разрушение коллагена и фибронектина (высокомолекулярный белок соединительной ткани). При идиопатическом фиброзе отмечается преобладание фиброза при не выраженных воспалительных изменениях. Основным механизмом прогрессирования пневмофиброза является постоянное повреждение эпителия альвеол с нарушением его регенерации и избыточным отложением соединительной ткани в связи с активацией фибробластов.
Общая информация
Течение патологии характеризуется тем, что у человека нет сопутствующей урогенитальной инфекции. Болезнь считается хронической, то есть у пациента бывают периоды обострений и ремиссии.
Интерстициальный цистит является тяжело диагностируемой формой воспаления мочевого пузыря.
Механизм возникновения окончательно не изучен, но медики выделяют несколько гипотез.
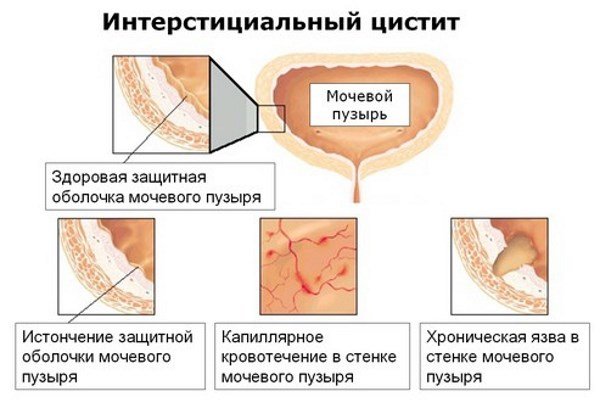
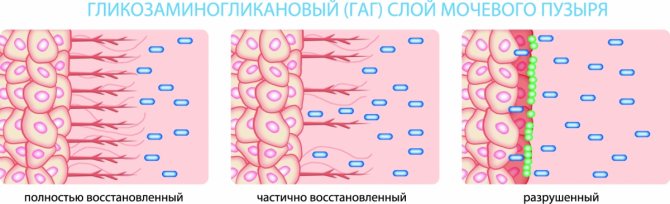
Механизм развития интерстициального цистита основан на том, что в некоторых участках стенки мочевого пузыря истончается слизистая оболочка.
Как результат, не выполняет главную функцию — защиту мышечного слоя от агрессивных компонентов мочи.
На ранних стадиях болезни отмечается воспаление всей стенки мочевого пузыря, в дальнейшем, воспаление из катаральной переходит в язвенную, что формирует структурный дефект.
При отсутствии лечения, этот дефект приводит к перфорации, что грозит развитием перитонита. Для брюшной полости моча является агрессивной средой.
При попадании в абдоминальную полость, возникают тяжелые нарушения в работе кишечника и других органов, которые там расположены.
Классифицировать цистит можно в зависимости от тех факторов, которые провоцируют:
- медикаментозный (следствие приема лекарств);
- механический (травмирование или оперативное вмешательство на мочевом пузыре);
- токсический;
- химический (следствие употребления химиопрепаратов);
- алиментарный (пищевого происхождения).
Прогноз
Прогноз и продолжительность жизни при фиброзе легких зависит от заболевания, на фоне которого он развился, степени прогрессирования самого фиброза, его протяженности и степени вовлечения бронхиального дерева (имеется в виду формирование бронхоэктазов, которые утяжеляют течение заболевания). Среди прогностических критериев главным является тип формирования пневмофиброза.
К благоприятным типам относятся фиброзные изменения в виде тяжей в центральном и периферическом интерстиции легких, а также ателектатический тип фиброза. Последний формируется в местах организовавшейся пневмонии или на месте длительно существовавшего спадения легочной ткани в результате закрытия бронхов. Возникновение этих типов пневмофиброза не влияет на перфузию и диффузию в легких и не приводит к развитию дыхательной недостаточности. К неблагоприятным типам относятся изменения в виде ацинарного фиброза и «сотового легкого», которые всегда приводят к нарушению перфузии и выраженной дыхательной недостаточности. Именно она является фактором, который уменьшает продолжительность жизни больного.
«Сотовое легкое» и значительная его распространенность считаются самым неблагоприятным прогностическим признаком. При этом придается значение и размеру «сот» — более неблагоприятными считаются «соты» большого размера или смешанный тип строения с чередованием мелких и крупных кист. Что касается их локализации, то неблагоприятным считается нижнезональное расположение.
Естественное течение идиопатического фиброза связано с постепенным изменением легочной ткани и прогрессирующим фибротическим повреждением, которое на конечной стадии приобретает вид «сотового легкого». Нарастающий фиброз прогрессивно ухудшает состояние больного и влияет на продолжительность жизни.
Трудно ответить на вопрос, сколько живут при этом заболевании, поскольку это зависит от состояния легочной функции. Сроки могут колебаться от 2 до 6 лет. Так, при остром течении больные живут не более 2 лет, при подостром – от 2 до 4 лет, а при хроническом – от 4 до 6 лет. Усугубляет положение сопутствующие заболевания, возникающие с возрастом. Летальный исход вызывает не только развитие острой дыхательной недостаточности, но и ИБС, тромбоэмболия легочной артерии или рак легкого.
При медленно прогрессирующем силикозе прогноз для жизни положительный, поскольку процесс перехода одной стадии в другую может длиться десятки лет. Бывают случаи, когда прогрессирование фиброза вообще не обнаруживается — в таких случаях прогноз для жизни благоприятен. Тяжелое осложнение силикоза — спонтанный пневмоторакс, но он встречается очень редко при современных формах силикоза. Если на фоне силикотического фиброза развивается туберкулез, то течение болезни неблагоприятное и в целом прогноз зависит от выраженности туберкулеза и силикоза, и формы туберкулеза.
Симптомы и признаки
Симптомы интерстициального нефрита у взрослых могут протекать различно. Опишем клинические признаки на примере острого процесса, который вызван лекарственным этиологическим фактором. В качестве примера возьмем инфекционное заболевание, например, острый бронхит, по поводу которого назначается антибактериальная терапия.
После введения антибиотиков (как правило, впервые в организм вводится данный антибиотик, либо его доза значительно выше, чем ранее, достигая уровня нефротоксичности), в течение нескольких дней у пациента возникает вторая волна лихорадки, которая никак не прогнозируется и не сочетается с усилением хрипов в лёгких, и, по-видимому, вызвана другими причинами.
После второй лихорадочной волны у пациента возникают симптомы интерстициального нефрита: появляются боли в пояснице, а также появление крови в моче вместе с белком. Это показатели так называемого мочевого синдрома, и на фоне гематурии и протеинурии возникают признаки острой почечной недостаточности.
Падает скорость клубочковой фильтрации, в плазме крови растёт уровень креатинина, пациент выделяет большое количество мочи с низкой концентрацией, и таким образом ОПН чаще всего сразу проявляется полиурической стадией. Подробнее о развитии острой почечной недостаточности читайте здесь.
Другими проявлениями острого мочевого синдрома является появление эритроцитов в моче, лейкоцитурия и особенно появление в мочевом осадке эозинофилов. При тяжёлом течении может возникать и анурия, практически у 30% пациентов наблюдается резкое повышение артериального давления в виде острого гипертензионного синдрома. Для таких пациентов нехарактерен отечный синдром.
Существуют и внепочечные проявления острого тубулоинтерстициального нефрита. Чаще всего — это диффузные боли в суставах, пояснице, появление сыпи (
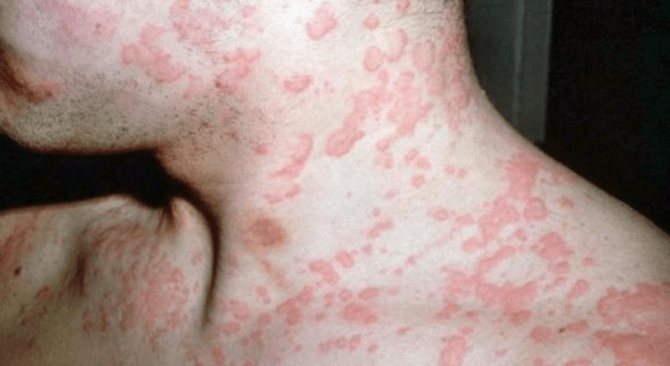
). В лабораторных исследованиях ваявляется лейкоцитоз в крови и эозинофилия. Довольно часто у пациентов боли в почках связаны с развитием почечной колики, а она, в свою очередь, обусловлена некрозом сосочковый зоны почек, куда открываются собирательные трубочки.
Старыми клиницистами описана так называемая классическая триада, характерная для тубулоинтерстициального поражения в острой форме. Это лихорадка, кожная сыпь и диффузные боли в суставах. В настоящее время такая клиническая картина, сопровождаемая выраженным мочевым синдромом, развивается не чаще, чем в 20% случаев.
Патогенез.
Дезорганизация альвеолярной архитектоники — характерный признак
большинства форм ИЗЛ, — обусловлена хроническим воспалением дистальных отделов
респираторного тракта.
В случаях ИЗЛ установленной этиологии хронический воспалительный процесс
индуцируется известными агентами. При этом (например, при лекарственно-зависимой
патологии легких) причинные факторы, обладая цитотоксическим эффектом, оказывают
непосредственное повреждающее действие на легочную ткань. Среди ИЗЛ неизвестной
этиологии воспаление играет меньшую роль, и в основе повреждения и
дезорганизации легочной ткани лежат патологическая пролиферация мезенхимальных
клеток (например, при лимфангиолейомиоматозе) либо отложение депозитов
внеклеточного материала, в норме отсутствующего в респираторных отделах легких
(например, при альвеолярном протеинозе).
Различают два основных механизма повреждающего действия клеток воспаления на
альвеолы. Первый заключается в том, что клетки воспаления аккумулируются на
ограниченных участках альвеолярной стенки, а это приводит к ее повреждению и
нарушениям процесса газообмена. Второй предполагает выделение воспалительными
клетками большого числа медиаторов, повреждающих клетки паренхимы и
соединительнотканный матрикс, стимулирующих пролиферацию фибробластов, что и
приводит к формированию легочного фиброза.
В норме в одной альвеоле содержится около 60 альвеолярных макрофагов и 15
лимфоцитов, тогда как полиморфно-клеточные лейкоциты, как правило, не
обнаруживаются. При развитии же воспаления (в случае интерстициальных
заболеваний легких неясной этиологии) происходят следующие морфологические
изменения: 1) значительно увеличивается число клеток воспаления в респираторных
отделах легких; 2) изменяется соотношение воспалительных клеточных элементов —
для одних заболеваний характерно преобладание лимфоцитов, в других случаях
доминируют нейтрофилы, альвеолярные макрофаги и/или эозинофилы; 3) повышается
функциональная активность клеток воспаления. Последние активируются под
воздействием целого ряда медиаторов, которые в свою очередь оказывают
повреждающее действие на альвеолярные структуры. Так, некоторые медиаторы
инициируют процесс образования токсичных кислородных радикалов, которые вызывают
повреждение клеток паренхимы; высвобождающиеся при этом внутриклеточные протеазы
обусловливают дезорганизацию соединительнотканного матрикса легких.
Легочный фиброз развивается вследствие высвобождения альвеолярными макрофагами
медиаторных субстанций, инициирующих пролиферацию фибробластов. Эти медиаторы,
включая фибронектин и ростовой фактор альвеолярных макрофагов, способствуют
перемещению фибробластов в интерстиций. В результате резко увеличивается число
фибробластов, «продуцирующих» соединительную ткань, что и приводит к
формированию пневмофиброза.
Хотя представленные механизмы и являются достаточно специфичными для
идиопатического легочного фиброза, последний может рассматриваться в качестве
своеобразного образца развития и прогрессирования легочного фиброза для всей
группы ИЗЛ в целом. Обозначения: AMDGF — ростовой фактор альвеолярных
макрофагов.
При некоторых заболеваниях, относимых в рубрику ИЗЛ, в патологический процесс
вовлекаются также мелкие легочные артерии и вены. При этом в редких случаях
проявления легочного васкулита оказываются доминирующими, преобладая над менее
выраженными паренхиматозными изменениями. Иногда воспалительный процесс
ограничивается терминальными бронхиолами, что препятствует движению воздуха к
соответствующим альвеолам; с другой стороны, для отдельных форм ИЗЛ характерно
поражение висцеральной плевры с развитием плеврального выпота.
Классификация
По распространенности и рентгенологическим или КТ признакам:
- Локальный фиброз легких (ограниченный). Локальный пневмофиброз поражает только часть легочной ткани, которая становится более плотной. На снимках четко определяются границы патологического процесса. Ограниченный пневмофиброз не влияет на эластичность всего легкого и на функции дыхания почти не отражается. Протекает бессимптомно и чаще не беспокоит пациентов. Примером ограниченного фиброза может быть исход крупноочаговой пневмонии. При хроническом бронхиолите при рентгенологическом исследовании обнаруживаются, помимо локального пневмосклероза, еще и утолщения вокруг бронхов. При этом заболевании обычно встречаются двусторонние фиброзные изменения в нижних отделах.
- Диффузный. При этом варианте фиброз диффузно охватывает всю легочную ткань и распространение процесса происходит намного быстрее, чем при локальной форме. Ткань легких уплотняется, структура деформируется и уменьшается объем легких. В связи с этим функция дыхания значительно ухудшается.
- Очаговый фиброз легких – наличие нескольких разных по размерам и структуре очагов. Они могут быть как ограниченные (округлой формы) и диффузные (размытые, без четких границ). Очаговый пневмофиброз выявляется при силикозе, пневмокониозе, на месте расположения гранулем различного происхождения.
- Линейный фиброз легких. При какой патологии он встречается и что это значит «линейный пневмофиброз»? Этот термин применяется для описания рентген-обследования или КТ легких, если выявляется уплотнение ткани в виде тяжа линейной формы (практически это рубец, который имеет линейную форму). Образуется такой вид фиброза после воспалительных заболеваний (прежде всего — туберкулез), травм, оперативных вмешательств. Линейная патология часто проявляется на рентгенограмме только через несколько лет после перенесенной болезни. Участок линейного фиброза, который связан с корнем лёгких, свидетельствует о перенесенной прикорневой пневмонии или первичном туберкулёзном комплексе. При хронической форме экзогенного альвеолита КТ-проявлениями являются: ячеистый и грубый линейный фиброз. При идиопатическом фиброзе поражение паренхимы симметричное, при этом в зависимости от стадии очень часто отмечается линейный фиброз, «матовое стекло», бронхоэктазы и «сотовое легкое».
- Перибронховаскулярный фиброз — наличие соединительной ткани вдоль бронхососудистого пучка. При этом просвет бронхов и сосудов сужается, что вызывает вентиляционные и сосудистые нарушения.
- Ацинарный (внутридольковый) — процесс отражает заполнение ацинусов и терминальных бронхиол клетками соединительной ткани. При этой форме отмечаются выраженные перфузионно-диффузионные нарушения. Так проявляется на КТ интерстициальная пневмония.
- «Сотовое легкое» — полная утрата нормального строения легкого. В легочной ткани отмечается чередование полей фиброза, эмфиземы и кист, что напоминает пчелиные соты.
По течению:
- Прогрессирующий.
- Не прогрессирующий.
Отдельно выделяется идиопатический фиброз легких — особая форма/вариант хронической фиброзирующей интерстициальной пневмонии неизвестной этиологии, которая неуклонно прогрессирует и является причиной смертности. Возникает преимущественно у людей старшего возраста и поражает только легкие. Процесс чаще локализуется в периферических отделах легких и проявляется интерстициальным воспалением альвеол с формированием вокруг альвеолярных ходов фиброза.
Как сказано выше, причины заболевания неизвестны, но выделяют факторы, которые усугубляют идиопатический легочный фиброз — это курение, вдыхание неорганической и органической пыли, вирусная инфекция, сахарный диабет. Заболевание чаще всего встречается у пациентов в возрасте старше 50 лет. Частота заболевания увеличивается с возрастом и преобладает после 60–70 лет.
Диагностика
Определение причины интерстициальных заболеваний лёгких может представлять собой трудную задачу, поскольку список возможных расстройств, способных вызывать проблемы, очень широк. К тому же, целый ряд других медицинских состояний имеет аналогичные признаки и симптомы, поэтому врачам приходится исключать их перед постановкой окончательного диагноза.
Ниже приведены экспертизы, которые обычно используют врачи для диагностики ИЗЛ.
Лабораторные анализы
Анализы крови. Определённые анализы крови могут выявить белки, антитела и другие маркеры аутоиммунных заболеваний или воспалительных реакций организма на воздействие факторов внешней среды.
Визуализированные диагностические процедуры
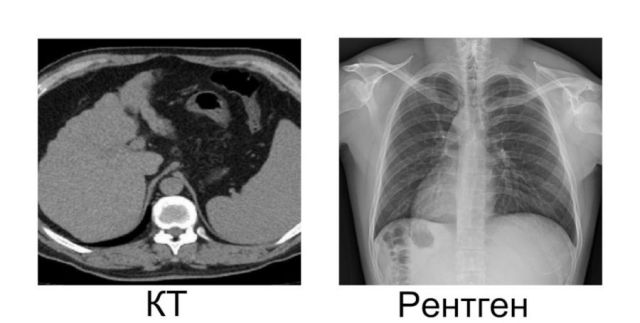
При диагностике ИЗЛ врач может порекомендовать компьютерную томографию
- Компьютерная томография (КТ). Данный метод исследования является ключевым, а иногда первым шагом при диагностике интерстициальных заболеваний лёгких. При КТ используется компьютер в комбинации с рентгеновскими снимками, сделанными под несколькими углами для получения изображений внутренних структур в поперечных сечениях. Компьютерная томография высокого разрешения может оказаться особенно полезной при определении степени повреждения лёгких. Она более детально показывает фиброз, а это может принести пользу при сужении диагноза и принятии решений относительно терапевтических стратегий.
- Эхокардиография. Эхокардиография предполагает использование звуковых волн для визуализации сердца. Данный диагностический метод даёт возможность получить изображения структур сердца и видео, которые позволяют узнать, как этот орган функционирует. При помощи эхокардиографии врачи также могут оценить величину давления в правой стороне сердца.
Тесты для оценки работы дыхательной системы
- Спирометрия. Во время данной процедуры пациент быстро и сильно выдыхает в специальную трубку, присоединённую к устройству, которое измеряет, сколько воздуха могут удерживать лёгкие и насколько быстро пациент способен выдыхать из них воздух. Спирометрия также позволяет оценить, насколько легко кислород перемещается из лёгких в кровоток.
- Оксиметрия. Это простой тест, который предполагает помещение специального устройства на пальцы для измерения насыщения крови кислородом. Оксиметрия может быть выполнена в состоянии покоя или при совершении физической активности. Она позволяет оценить степень тяжести и течение заболеваний лёгких.
Анализ лёгочной ткани
Во многих случаях лёгочный фиброз может быть окончательно диагностирован только путём проверки небольшого количества лёгочной ткани (биопсии) в лаборатории.
Ниже приведены три способа, при помощи которых может быть взят образец ткани на анализ.
- Бронхоскопия. В рамках данной процедуры врач удаляет очень маленький образец ткани (обычно не больше шляпки гвоздя), используя тонкую гибкую трубку (бронхоскоп), которая через нос или рот вводится в лёгкие. Бронхоскопия, как правило, связана с минимальными рисками — чаще всего от использования бронхоскопа наблюдается только временная болезненность горла и охриплость. Однако иногда объём взятой на анализ ткани оказывается слишком маленьким для точной диагностики.
- Бронхоальвеолярный лаваж. В рамках этой процедуры врач при помощи бронхоскопа вводит в лёгкие приблизительно столовую ложку подсоленной воды, а затем сразу же удаляет раствор. Полученная жидкость содержит клетки альвеол пациента. Притом что бронхоальвеолярный лаваж отбирает образцы из значительно больших участков лёгких по сравнению с другими диагностическими процедурами, он часто не даёт врачам достаточно информации для диагностики лёгочного фиброза.
- Хирургическая биопсия. Хотя это более инвазивная процедура, связанная с потенциальными осложнениями, она часто становится единственным вариантом, который позволяет врачам получить достаточно большие участки тканей для постановки точного диагноза. Когда пациент находится под общей анестезией, хирург выполняет два или три небольших разреза между рёбрами и вводит туда хирургический инструмент с камерой. Камера позволяет врачу рассмотреть лёгкие на мониторе и удалить образец лёгочной ткани.
Этиология
Этиопатогенетические особенности заболевания в настоящее время до конца не изучены. Специалисты до сих пор задаются вопросом, почему воспалительный процесс завершается не заживлением, а образованием соединительнотканных тяжей в легких. Существует несколько теорий происхождения неспецифической интерстициальной пневмонии: аутоиммунная, инфекционная, генетическая, аллергическая, токсическая и некоторые другие.
- Одной из причин болезни является нарушение иммунного гомеостаза – расстройство иммунологической саморегуляции. В организме человека вырабатываются антитела к собственным клеткам, которые воспринимаются как чужеродные. Формируются иммунные комплексы, циркулирующие в крови и вызывающие развитие аутоиммунного воспаления.
- Инфекционная теория болезни связана с проникновением в организм патогенных микробов: вирусов – цитомегаловируса, герпес-вируса; грибков — кандиды, аспергиллы; внутриклеточных микроорганизмов – микоплазмы, хламидии; бактерий – пневмококков, синегнойной или гемофильной палочек. Микробы проникают в организм воздушно-капельным путем и поражают межуточное вещество легочной ткани. В данном случае возбудитель не играет первостепенного значения. Реакция организма идет не по пути классического воспаления. Чаще всего патология развивается из-за неинфекционных причин.
- Курение способствует поражению легочной ткани и развитию респираторного бронхиолита. У курильщиков «со стажем» патология протекает тяжело, часто осложняется и плохо поддается лекарственной терапии.
- Негативные внешние факторы приводят к воспалению интерстициальной ткани — пылевые частицы, аллергены, химические аэрозоли, токсические газы.
Факторы, предрасполагающие и провоцирующие развитие пневмонии:
- Иммунодефицит, обусловленный гормонотерапией или химиотерапией, тяжелыми соматическими заболеваниями,
- Запыленный и загазованный воздух на производстве,
- Негативное воздействие на респираторный тракт бытовых раздражителей,
- Кардиоваскулярные расстройства,
- Врожденные пороки развития органов дыхания,
- Хронические фоновые патологии,
- Длительный прием некоторых медикаментов, предназначенных для борьбы с аритмиями, ревматизмом и прочими недугами,
- Возраст старше 60 лет,
- Наследственная предрасположенность,
- Сахарный диабет,
- Печеночная дисфункция,
- Операции по пересадке органов и тканей,
- Гнойно-бактериальные процессы,
- ВИЧ и СПИД,
- Иммунопатии, коллагенозы.
В основе заболевания лежит иммунное неинфекционное воспаление альвеол — основных структурных единиц легочной ткани. В пораженных альвеолярных стенках и межуточной ткани органа скапливаются иммунокомпетентные клетки. Они выделяют биологически активные вещества, повреждающие структуры легких и фиброгенные факторы, запускающие фибропролиферативные процессы.
Лечение интерстициального цистита
ИЦ/СБМП сложно поддаётся лечению. Лечебная тактика основывается на консервативном лечении, изменении образа жизни и питания. Дополнительно может применяться фитотерапия. А в тяжёлых случаях показано хирургическое вмешательство.
Медикаментозное лечение
При ИЦ/СБМП обычно назначают:
- Антидепрессанты трициклической группы, такие как Амитриптил для уменьшения гиперактивации нервов в стенке МП;
- Антибактериальный препарат Габапентин для лечения боли;
- Антигистаминные препараты, например, Лоратадин для снятия симптомов аллергии и Гидроксизин для облегчения сна;
- Феназопиридина гидрохлорид способен облегчить боли в МП, срочность, частоту мочеиспускания и жжение.
Иногда люди самостоятельно используют Ибупрофен или Аспирин для снятия лёгкого дискомфорта. Но с ними нужно быть осторожнее, так как данные средства могут ухудшить симптомы.
Растягивание мочевого пузыря
Мы уже писали выше о том, что некоторые пациенты отмечают улучшение состояния после процедуры растяжения МП, проводимого при цистоскопии.
Иногда медицинские работники растягивают МП при помощи гидробужирования — накачивания органа водой. Исследования показывают, что улучшения отметили от 40 до 80% пациентов. Положительный эффект длится от нескольких недель до полугода, хотя у некоторых пациентов симптоматика временно ухудшается сразу после гидробужирования. Процедура проводится с применением тяжёлых седативных препаратов или под наркозом.
Инстилляция мочевого пузыря
Инстилляции мочевого пузыря при цистите проводятся при помощи катетера. Медицинские работники вводят узкую трубку в уретру, сливают мочу, а затем заливают лечебные растворы, такие как:
- Диметилсульфоксид,
- Натрия бикарбонат,
- Гепарин,
- Гидрокортизон.
Другие методы
Если пациент плохо реагирует на медикаментозную терапию, растяжение МП или инстилляцию, рекомендуются другие методы терапии:
- Сакральная нейромодуляция. Суть процедуры в имплантации устройства для стимуляции нервов сакральной области (нижняя часть спины). Метод работает путём подавления гиперактивных сигналов, которые подают сенсорные нервы в стенке МП.
- Чрескожная электрическая стимуляция нервов (ЧЭСН). Это тоже форма нейромодуляции, не требующая хирургического размещения импульсного генератора и проводов. Через провода, которые располагаются между пупком и лобком, на коже нижней зоны спины или через специальные устройства, вставленные в прямую кишку у мужчин и во влагалище у женщин, в тело проникают мягкие электрические импульсы. Длительность — от нескольких минут до нескольких часов, частота — 2 или более раз в день.
Клиницисты считают, что электрические импульсы способствуют:
- увеличению притока крови к МП;
- укреплению тазовых мышц;
- выбросу гормонов, блокирующих боль.
ЧЭНС более эффективно снимает болевой синдром, но менее действенна в отношении частоты мочеиспускания.
Хирургическое лечение
Хирургическое вмешательство проводится редко и показано при тяжёлом ИЦ/СБМП.
Хирурги выполняют:
- периферическую денервацию (надрез нервов к стенке МП и от неё);
- увеличение МП для увеличения его ёмкости;
- цистэктомию — полное удаление МП и пластикой нового органа из тканей собственного толстого кишечника.