Что такое резистентность и какова ее роль, инсулинорезистентность и невосприимчивость бактерий к антибиотикам
Содержание:
- Поколения и резистентность
- Методы борьбы с резистентностью к антибиотикам
- Диффузионные методы
- Что такое устойчивость к антибиотикам?
- Высокий уровень приоритетности
- Что делать?
- Проблема антибиотикорезистентности
- Правила приема антибиотиков
- Глубина проблемы резистентности
- Что такое резистентность?
- Как и почему возникает резистентность
Поколения и резистентность
Существует 4 поколения антибактериальных медикаментов. Последнее поколение демонстрирует наибольшую эффективность. В структуре противомикробных таблеток или уколов находится множество сложных элементов. Препараты 4 поколения обладают не только большей лекарственной эффективностью, но и менее токсичны для организма.
Средства последнего поколения принимаются меньшее количество раз в день. Эффект от их использования достигается гораздо быстрее. С их помощью возможно вылечить хроническое заболевание. Ингибирование ферментов микроба у современных препаратов очень высокая. При правильных действиях медикаменты последнего поколения будут эффективны несколько десятилетий.
В больницах часто назначают лекарства 3 и 4 поколения. Простые заболевания поддаются терапии при использовании препаратов 3 поколения. Они обладают большей токсичностью, но приобретаются в аптеке по более выгодной цене. Современное поколение не так широко распространенно и имеет стоимость выше, чем у более устаревших аналогов. Прием самого современного лекарства не всегда целесообразен. Пользоваться необходимо тем медикаментом, который оказывает нужный эффект. Если пренебрегать этим правилом, вызывается резистивность к современным лекарствам.
Пока еще микробы не имеют резистентность к антибиотикам последнего поколения. Хотя в условиях больниц и мест скопления различных патогенных микроорганизмов уже ходят слухи о том, что существуют невероятно устойчивые штаммы стафилококков и стрептококков. Со слов ученых антибиотикорезистентность способна развиваться бесконечно. Более того, об этом процессе было известно до появления первого антибиотика. Это глобальная проблема, так как создавать эффективные препараты все сложнее. Резистентность — особенность живых организмов. Это значит, что, в данный момент создать лекарство, к которому не будет привыкания — невозможно. Однако ученые двигаются в сторону изобретения идеального медикамента. Скорее всего, это будет абсолютно новый класс лекарств.
Принципы применения для предотвращения резистентности
От правильных действий человека зависит, как быстро микробы будут развиваться. Если будет вестись беспорядочный прием противомикробных медикаментов, в нужный момент лекарство просто не подействует. Любые антибиотики по механизму своего действия со временем вызывают резистентность.
Выделяют следующие правила приема антибиотиков:
- всегда заканчивать курс, даже если наступило улучшение;
- принимать медикамент по инструкции или рекомендациям врача;
- после приема проводить профилактику дисбактериоза;
- избегать самостоятельного назначения и использования антибактериальных препаратов.
Если соблюдать это, удастся повысить пользу от терапии и снизить частоту возникновения побочных эффектов. Если микробы будут уничтожены, то резистентность не передастся новым микроорганизмам. Стоит понимать, что соблюдение норм приема антибиотиков необходимо, чтобы при столкновении с серьезной болезнью (бактериальная пневмония, менингит) воздействовать на патогенные инфекции и возбудителей.
Методы борьбы с резистентностью к антибиотикам

Сегодня борьба за место под солнцем идет во всех возможных направлениях. Прежде всего, конечно следует по возможности ограничить и жестко контролировать применение антибиотиков. По статистике, треть назначаемых врачами антибиотиков не нужны пациентам, то есть следует более аккуратно использовать их при лечении. Но, кроме того, человек изобретает, комбинирует и ищет новых врагов для убивающих его бактерий.
Разработка новых антибиотиков.
Увы, это один из самых мало перспективных методов борьбы с антибиотикорезистентностью. Любые лекарства, какими бы они сильными не были, рано или поздно окажутся бесполезными — пример колистина это демонстрирует более чем наглядно. Поэтому новые, неизвестные ранее лекарства появляются все реже и реже. Хотя иногда ученым удается найти что-нибудь интересное. Например, недавно из морской антарктической губки было выделено вещество дарвинолид, которое уничтожает до 98% клеток золотистого стафилококка.
Комбинированные методы лечения.
Это самый распространенный путь лечения пациентов с МЛУ-инфекциями. Правильно подобранная комбинация уже известных препаратов не оставляет бактериям шансов на выживание — а значит и на появление устойчивых к ним штаммов. Например, в июне 2016 года фармацевты сообщили о создании нового, комбинированного препарата (из цефдинира и ТХА709), который эффективно уничтожает метициллин-резистентный золотистый стафилококк. Еще один пример — комбинация некоторых пенициллинов с клавулановой кислотой. Последняя способствует разрушению клеточной стенки, а уже после этого в дело вступают антибиотики.
«Враг моего врага…»
Идет поиск и «натуральных» методов борьбы с патогенными микробами. Например, существуют вирусы, которые питаются бактериями, они так и называются — бактериофаги. Эти микроорганизмы были обнаружены еще в конце XIX века. Но, увы, панацеей в данном случае они быть не могут. Во-первых, они очень узко специализированы и не интересуются другими бактериями, кроме конкретного штамма. Во-вторых, микробы и к ним научились быть резистентными.
А в прошлом году немецкие исследователи сообщили о бактериях Staphylococcus lugdunensis, которые и сами умеют вырабатывать антибиотик, опасный для золотистого стафилококка с МЛУ. Оказалось, что чудесные бактерии обитают в носовой полости человека. Вещество люгдунин, которое они производят, подавляет рост опасного микроорганизма.
Диффузионные методы

Анализ мочи на чувствительность к антибиотикам, и не только ее, можно провести несколькими способами. Первый из них – это метод дисков. Проводят его следующим образом. В чашку Петри заливают агар, а когда он застынет, специальным инструментом наносят исследуемый материал. Затем по поверхности агара раскладывают бумажные диски, пропитанные антибиотиками. После чашку закрывают и ставят в термостат. Постепенно диск погружается в желатин, а антибиотик диффундирует в окружающее пространство. Вокруг бумаги образуется зона «подавления роста». Чашки проводят в термостате двенадцать часов, затем их вынимают и измеряют диаметр вышеуказанной зоны.
Второй способ – это метод Е-теста. Он похож на предыдущий, но вместо бумажных дисков используют полоску, которая на своем протяжении в разной степени пропитана антибиотиком. После двенадцати часов экспозиции в термостате чашку Петри достают и смотрят, в каком месте зона подавления роста соприкасается с полоской бумаги. Это будет наименьшая концентрация препарата, которая необходима для лечения заболевания.
Достоинством этих тестов является быстрота и простота их проведения.
Что такое устойчивость к антибиотикам?
Представьте себе ситуацию, когда программист борется с хакером. Чем более совершенную антивирусную программу создаст ИТ-специалист, тем более сложные вирусы будет создавать хакер. После каждого нового вируса, который проник в систему и не был обнаружен и удален существующей антивирусной программой, ИТ-специалист должен подготовить улучшенный алгоритм. Когда на рынке появляется последняя антивирусная программа, хакеры уже начинают работать над другим вирусом, устойчивым к этой программе.
Устойчивость к антибиотикам – аналогичное явление, только оно возникает, когда бактерии приобретают устойчивость. Чем лучше и эффективнее антибиотик представлен на рынке, тем больше бактерий сосредоточено на изменении своих свойств, нейтрализующих свойства нового препарата. Так возникает устойчивость к антибиотикам.
С этой целью бактерии могут изменять свой генетический материал таким образом, что устойчивость к новому антибиотику становится их постоянной характеристикой, передаваемой будущим поколениям. Если с последующей серией лекарств, созданных учеными, бактерии приобретают устойчивость к воздействиям, то мутации в бактериальной ДНК накапливаются и образуют бактериальные штаммы, устойчивые практически к большинству антибиотиков. Этот процесс является основой бактериальной устойчивости к антибиотикам.
Устойчивость к антибиотикам
Высокий уровень приоритетности
- Enterococcus faecium
- Staphylococcus aureus
- Helicobacter pylori
- Campylobacter spp.
- Salmonellae
- Neisseria gonorrhoeae
Бактерии второй группы объединены по признаку повсеместного распространения, высокой социально-экономической значимости вызываемых ими заболеваний и быстрого развития резистентности к основным антибиотикам, используемым для их эрадикации, однако в резерве еще остается один или несколько эффективных препаратов.
Enterococcus faecium
E. faecium входит в состав нормальной микрофлоры кишечника, но в то же время является условно-патогенным микроорганизмом. У ослабленных больных может вызывать инфекции мочевыводящих путей, раневую инфекцию, сепсис и эндокардит. Резистентен к аминогликозидам, пенициллинам и цефалоспоринам. Беспокойство вызывает снижение чувствительности к ванкомицину — до 72 % в отдельных популяциях. Большинство штаммов E. faecium чувствительны к линезолиду, тигециклину, даптомицину.
Staphylococcus aureus
Золотистый стафилококк, колонизирующий кожу и слизистые оболочки, способен вызывать тяжелые инфекции кожи и мягких тканей, респираторные, раневые инфекции, остеомиелит, сепсис, артрит, эндокардит. Недавнее появление и распространение ванкомицин- и гликопептид-резистентных штаммов в дополнение метициллин-резистентному S. aureus значительно сужает выбор антибактериальных препаратов, однако у возбудителя сохраняется чувствительность к аминогликозидам, эритромицину, тетрациклину, ко-тримоксазолу, линезолиду.
Helicobacter pylori
Тревогу ВОЗ вызывает увеличение случаев резистентности всем известной H. pylori к кларитромицину, что сказывается на эффективности традиционных схем эрадикационной терапии, в том числе и в России. Перед эрадикацией ВОЗ рекомендует проверить чувствительность бактерии к этому антибиотику, при выявлении устойчивости — использовать схемы без него — с метронидазолом, тетрациклином или рифаксимином, а также добавлять висмута трикалия дицитрат.
Campylobacter spp.
Бактерии рода Campylobacter удерживают первое место в мире по гастроэнтеритам, которые у большинства населения планеты протекают в легкой форме, но представляют опасность для маленьких детей, беременных, стариков и иммунокомпрометированных больных. В большинстве случаев достаточно регидратации и восстановления электролитного баланса, антибактериальную терапию назначают при тяжелом течении. Проблемой является резистентность Campylobacter к фторхинолонам, основному средству борьбы с кишечной микрофлорой, и макролидам. Устойчивость к этим препаратам, впрочем, сильно варьирует от страны к стране — от менее 5 % в Финляндии до более 90 % в Индии. В Европе и России эритромицин всё еще остается препаратом выбора. По данным микробилогических исследований, в России также еще вполне актуальны фторхинолоны. В запасе для особо тяжелых случаев с осложнениями — гентамицин и карбапенемы.
Salmonellae
Представители рода сальмонелл также вызывают набор кишечных инфекций, от легкого энтерита до брюшного тифа. Большинство этих бактерий уже резистентны к бета-лактамам, аминогликозидам, тетрациклинам, хлорамфениколу и ко-тримоксазолу. Устойчивость к фторхинолонам растет во всем мире, но пока не привела к полной бесполезности этих препаратов, они остаются антибиотиками выбора, наравне с макролидами и цефалоспоринами третьего поколения. Антибактериальной терапии требуют только тяжелые случаи кишечных инфекций и, конечно, брюшной тиф и паратифы.
Neisseria gonorrhoeae
Гонорея из неприятной, но относительно легко излечимой болезни эволюционировала в глобальную медицинскую проблему. Гонококк потерял чувствительность к пенициллинам, тетрациклинам, сульфаниламидам и фторхинолонам.
Особое опасение вызывает появление и постепенное распространение штаммов, резистентных к цефалоспоринам (цефтриаксону), долгое время служивших безотказным средством борьбы с этой инфекцией. При резистентной к стандартным схемам лечения гонорее рекомендовано использовать комбинацию азитромицина с высокими дозами цефтриаксона. В России гонококк также практически резистентен к фторхинолонам, но пока сохраняет 100 %-ную чувствительность к цефтриаксону.
Что делать?
Так как проблема антибиотикорезистентности становится все более актуальной, научное сообщество прикладывает усилия к формированию новых принципов и методов лечения, позволяющих преодолеть сложность. Как правило, пользуются возможностями комбинированной терапии, но ей присущи определенные недостатки, и в первую очередь – повышенная частота побочных эффектов. Позитивный эффект в ряде случаев наблюдается при применении принципиально новых лекарств, показывающих хороший результат при резистентности штаммов к ранее примененным препаратам.
Чтобы стойкость микроорганизмов была преодолена, а эффективность терапевтического курса – повышена, разумно прибегать к проверенным комбинациям средств. Если выявлено заражение формами жизни, производящими бета-лактамазу, следует применять такие препараты, в составе которых есть компоненты, подавляющие активность фермента. К примеру, подобная особенность выявлена у клавулана, тазобактама. Эти вещества имеют довольно слабый антибактериальный эффект, но процесс ингибирования необратим, что позволяет защитить основной антибиотик от фермента. Чаще всего назначают клавулановую кислоту в комбинации с амоксициллином или тикарциллином. В аптеках такие препараты представлены под торговыми названиями «Аугментин» и «Тиментип». Еще один надежный препарат «Уназин» основан на ампициллине, защиту которому обеспечили через сульбактам.

Проблема антибиотикорезистентности
Отсутствие эффекта от антибиотикотерапии, связанное с антибиотикорезистентностью, приводит к тому, что болезнь продолжает прогрессировать и переходит в более тяжелую форму, лечение которой становится еще более затруднительным. Особую опасность представляют случаи, когда бактериальная инфекция поражает жизненно важные органы: сердце, легкие, головной мозг, почки и т.д., ведь в этом случае промедление смерти подобно.
Вторая опасность заключается в том, что некоторые болезни при недостаточности терапии антибиотиками могут приобретать хроническое течение. Человек становится носителем усовершенствованных микроорганизмов, устойчивых к антибиотикам определенной группы. Он же теперь является источником инфекции, бороться с которой старыми методами становится бессмысленным.
Все это подталкивает фармацевтическую науку к изобретению новых, более эффективных средств с другими действующими веществами. Но процесс опять идет по кругу с развитием антибиотикорезистентности уже к новым препаратам из разряда противомикробных средств.
Если кому-то кажется, что проблема антибиотикорезистентности возникла совсем недавно, он очень ошибается. Эта проблема стара как мир. Ну, возможно не настолько, и все же лет 70-75 ей уже есть. Согласно общепринятой теории, появилась она вместе с внедрением в медицинскую практику первых антибиотиков где-то в 40-х годах ХХ столетия.
Хотя существует концепция более раннего появления проблемы резистентности микроорганизмов. До появления антибиотиков этой проблемой особо не занимались. Ведь это так естественно, что бактерии, как и другие живые существа, старались приспособиться к неблагоприятным условиям окружающей среды, делали это по-своему.
Проблема резистентности болезнетворных бактерий напомнила о себе, когда появились первые антибиотики. Правда, тогда вопрос еще не стоял так актуально. В тот период активно велись разработки различных групп антибактериальных средств, что в некотором роде было обусловлено неблагоприятной политической обстановкой в мире, военными действиями, когда бойцы умирали от ранений и сепсиса лишь потому, что им не могли оказать эффективную помощь из-за отсутствия необходимых препаратов. Просто этих препаратов еще не существовало.
Наибольшее число разработок велось в 50-60 годах ХХ столетия, и в течение 2 последующих десятилетий велось их усовершенствование. Прогресс на этом не закончился, но начиная с 80-х годов разработок в отношении антибактериальных средств стало заметно меньше. Виной ли тому большая затратность этого предприятия (разработка и выпуск нового препарата в наше время доходит уже до границы в 800 миллионов долларов) или банальное отсутствие новых идей в отношении «воинственно настроенных» активных веществ для инновационных препаратов, но в связи с этим проблема антибиотикорезистентности выходит на новый пугающий уровень.
Занимаясь разработкой перспективных АМП и создавая новые группы таких препаратов, ученые надеялись победить множественные виды бактериальной инфекции. Но все оказалось не так просто «благодаря» антибиотикорезистентности, довольно быстро развивающейся у отдельных штаммов бактерий. Энтузиазм понемногу иссякает, но проблема так и остается нерешенной долгое время.
Правила приема антибиотиков
Джуди Сметзер, вице-президент американского Института безопасной практики медикаментозного лечения, говорит о пяти основных правилах приема лекарств, которые следует учитывать также и при приеме антибиотиков: правильный пациент должен получать правильное лекарство в правильное время в правильной дозе и правильным способом применения.
Какие еще правила следует соблюдать при лечении антибиотиками?
Самое важное правило — проводить лечение до конца и не уменьшать назначенные врачом дозировки. По данным российских исследований, каждая четвертая мама не доводит курс антибиотиков, прописанных ее ребенку, до конца
В то же время затягивать прием на более длительный срок тоже нельзя — это дает дополнительный шанс инфекции найти способ борьбы с препаратом. Только «золотая середина» способна эффективно остановить инфекцию.
Антибиотики узкого спектра, то есть действующие на ограниченное число бактерий, безопаснее и предпочтительнее препаратов широкого спектра
Чем точнее воздействие, тем меньше шансов на выживание патогенных бактерий.
В идеале перед назначением антибиотиков следует пройти обследование на чувствительность к тем препаратам, которые будут назначены.
Особое внимание при лечении антибиотиками в больницах следует уделить риску заражения внутрибольничными инфекциями. Это значит, что санитарная обработка и дезинфекция должны проводиться на максимально доступном уровне.
-
Практическое руководство по антиинфекционной химиотерапии / Под ред. Л.С. Страчунского, Ю.Б. Белоусова, С.Н. Козлова. Смоленск, 2007.
-
US woman dies of infection resistant to all 26 available antibiotics // MedicalXpress. 13.01.2017. -
Scientists examine bacterium found 1,000 feet underground // Еurekalert.org/ 8.12.2016. -
MRSA-killing antibiotic produced by bacteria in the nose // UPI. 27.07.2016. -
Researchers may have found second ‘superbug’ gene in U.S. patient // Reuters. 27.06.2016.
Глубина проблемы резистентности
Всю значительность проблемы показывает результаты опроса, инициированного ВОЗ. Так выяснилось, что две трети людей полагают: резистентным к антимикробным препаратам, становится именно человек. При этом:
- 65 процентов считают, будто антибиотик помогает от вирусов;
- 32% – лечение следует прекращать, как только наступает улучшение;
- 44% – резистентные бактерии создают сложности исключительно для людей, злоупотребляющих препаратами.
Никаких затруднений с устойчивостью возникнуть не может – медицина все решит, как только проблема достигнет серьезных масштабов. Так думают 64 процента опрошенных.
Статистика по России выглядит удручающе:
- 56% респондентов признали, что пили антибиотики в предшествующие 6 месяцев;
- из них только половине их назначил врач;
- 67% верят, будто антибиотики спасают от гриппа и других вирусов;
- 26% оставляют лечение после устранения симптомов.
Что такое резистентность?
Резистентность — это устойчивость микроорганизмов к действию антибиотиков. В организме человека в совокупности всех микроорганизмов встречаются устойчивые к действию антибиотика особи, но их количество минимальное. Когда антибиотик начинает действовать, вся популяция клеток гибнет (бактерицидный эффект) или вовсе прекращает свое развитие (бактериостатический эффект). Устойчивые клетки к антибиотикам остаются и начинают активно размножаться. Такая предрасположенность передается по наследству.
В организме человека вырабатывается определенная чувствительность к действию определенного рода антибиотиков, а в некоторых случаях и полная замена звеньев обменных процессов, что дает возможность не реагировать микроорганизмам на действие антибиотика.
Также в некоторых случаях микроорганизмы и сами могут начать вырабатывать вещества, которые нейтрализуют действие вещества. Такой процесс носит название энзиматической инактивации антибиотиков.
Те микроорганизмы, которые имеют резистентность к определенному типу антибиотиков, могут, в свою очередь, иметь устойчивость к подобным классам веществ, схожих по механизму действия.
Как и почему возникает резистентность
В природе резистентность появляется спонтанно из-за накапливающихся в ДНК случайных мутаций, которые повышают приспособленность микроорганизмов в среде с угнетающим веществом. Нередко это свойство приобретается и путем от других бактерий, поэтому детерминанты резистентности способны быстро распространяться даже между неродственными штаммами. При длительном воздействии антибиотика вначале погибает бόльшая часть популяции чувствительных к нему микроорганизмов, а та малая доля, что выживает, либо уже имеет жизненно важные для этих условий мутации, либо успевает мутировать или захватить нужные гены от бактерий-соседей и под селективным давлением антибиотика закрепить благоприобретения. В любом случае, выжившие способны нормально существовать и размножаться даже в присутствии антибиотика. То есть он больше на них не действует.
Нельзя сказать, что человечество не было осведомлено о способности микроорганизмов становиться резистентными к антибиотикам. Александр Флеминг, официально — первооткрыватель пенициллина , в своей нобелевской речи предупреждал о том, что препарат нужно использовать с умом и не позволять бактериям вырабатывать к нему устойчивость . Сегодня это утверждение необходимо распространить на все известные и применяемые в медицине и сельском хозяйстве антибиотики.
Уточняю, что «официально», потому что другие исследователи до Флеминга обнаруживали этот антибиотик; подробнее о предшественниках можно прочитать в обзоре «Эволюция наперегонки, или почему антибиотики перестают работать» , а о самом Флеминге — в статье «Победитель бактерий» .
Здесь стόит оговорить один момент. Обычно в быстро развивающейся резистентности бактерий винят людей, беспричинно принимающих антибиотики в «любой непонятной ситуации». Или людей, необоснованно прерывающих курс просто потому, что «стало лучше, чего лечиться-то» (рис. 1) . Тем не менее огромный вклад в это нехорошее дело вносит широкомасштабное использование антибиотиков в животноводстве: больше половины мирового объема используемых антибиотиков приходится именно на скотоводство и птицеводство . Подобная тактика сильно подрывает наши «рубежи» в борьбе с патогенными микроорганизмами. Причина добавления антибиотиков в корм для домашних животных проста и обоснована: они позволяют предотвратить ряд инфекционных заболеваний, поддержать здоровье и продуктивность животных, снизить смертность, которая оборачивается крупными экономическими потерями.
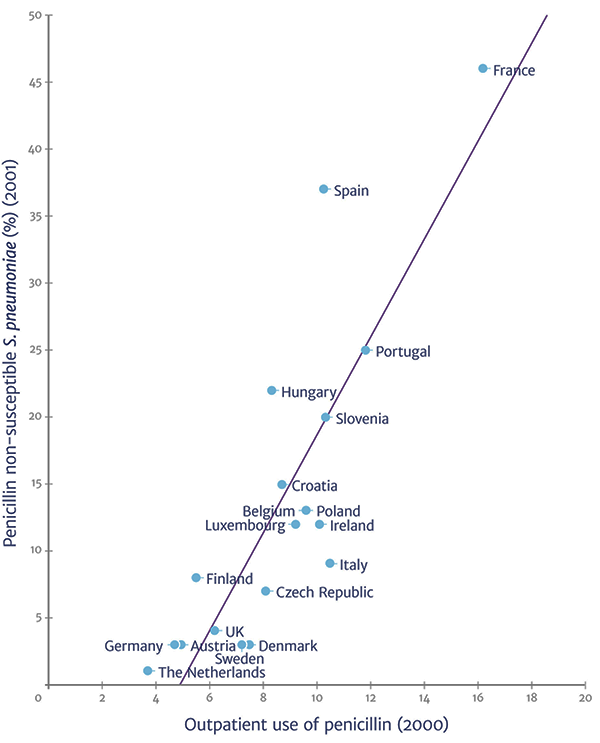
Рисунок 1. Существует прямая корреляция между использованием пенициллина и ростом доли устойчивых к нему пневмококков ().
В исследовании, опубликованном в журнале PNAS, подсчитали, что в 2010 году во всём мире в корма было добавлено более 63 000 тонн антибиотиков. И это — только по скромным оценкам. Ожидается, что к 2030 году указанное число возрастет на 67%, но, что должно особенно встревожить, оно удвоится в Бразилии, Индии, Китае, Южной Африке. И в России .
Побочным действием чрезмерного использования антибиотиков является то, что не все они метаболизируются. После выведения из организма они проникают в почву и задерживаются в ней, впоследствии накапливаясь в растениях. Через почву антибиотики попадают в воду и распространяются на значительные расстояния, воздействуя на бόльшее число микроорганизмов, чем изначально предполагалось. Они могут вновь попадать в организм человека и животных и воздействовать в том числе на их микробиом.
Таким образом, несмотря на многочисленные предупреждения, из-за массового и неправильного использования антибиотиков устойчивость к ним распространяется среди микроорганизмов всё шире и быстрее. А значит, людей и животных с каждым годом становится всё труднее лечить от бактериальных инфекций.